Les océans du Canada maintenant : Études de cas tirées du rapport sur l’état des mers arctiques du Canada, 2019
Les océans du Canada maintenant : Études de cas tirées du rapport sur l’état des mers arctiques du Canada, 2019
(PDF, 3.22 Mo)
Sur cette page
- Information sur le document
- Encadré : Les ours polaires et le déclin de la glace de mer
- Encadré : L’océan en fleur
- Encadré : Le phoque annelé et le déclin de la glace de mer
- Encadré : Une année différente
- Encadré : Sanctuaire de l’Arctique
- Encadré : Extension des aires de répartition
- Encadré : Points chauds de l’Arctique
- Encadré : Surveillance écologique par les collectivités
- Encadré : Intégration des connaissances
- Références Citées
Information sur le document
Sous la direction d’Andrea Niemi, Pêches et Océans Canada
Région du Centre et de l’Arctique
501, University Crescent
Winnipeg (Manitoba) R3T 2N6
Les études de cas sont tirées de :
Niemi, A., Ferguson, S., Hedges, K., Melling, H., Michel, C., et coll. 2019, État des mers arctiques du Canada. Rapp. tech. can. sci. halieut. aquat. 3344 : xv + 189 p.
© Sa majesté la reine du chef du Canada, représentée par le ministre des pêches et des océans du canada, 2019
No de cat.: Fs23-549/2-2019F-PDF
ISBN: 978-0-660-33145-4
Encadré : Les ours polaires et le déclin de la glace de mer
Réponse d’un superprédateur au déclin de l’habitat de la glace de mer dans l’ouest de la baie d’Hudson
Evan Richardson, Environnement et Changement climatique Canada

Figure 1. Ours polaire sur les rives de la baie d’Hudson (photo : Evan Richardson).
À l’échelle mondiale, la perte d’habitat représente l’une des plus grandes menaces pour la conservation des espèces. Dans l’Arctique, on prévoit que le déclin à long terme de l’étendue spatiale et temporelle de la glace de mer aura des répercussions importantes sur les espèces de mammifères marins dépendantes de la glace. Il y a près de 20 ans, les chercheurs ont commencé à voir les effets des changements climatiques sur l’ours polaire (Ursus maritimus) (Figure 1), le prédateur de niveau trophique supérieur le plus charismatique de l’Arctique. À ce moment-là, l’état corporel des ours polaires commençait à se détériorer dans l’ouest de la baie d’Hudson en raison de la réduction de l’étendue de la glace de mer et de la disponibilité de leurs principales proies, les phoques qui se reproduisent sur la glace (Stirling et coll. 1999). Des tendances semblables liées à l’état corporel des phoques annelés (Pusa hispida) et se rapportant à l’étendue de la glace de mer ont depuis été observées dans la baie d’Hudson (Ferguson et coll. 2017), indiquant ainsi que la glace de mer peut non seulement influencer la disponibilité des proies, mais aussi la qualité des proies consommées. Ces interactions interspécifiques importantes ont probablement joué un rôle prépondérant dans le déclin continu et à long terme de l’état corporel des ours blancs à la limite sud de leur aire de répartition (Obbard et coll. 2016; Sciullo et coll. 2016).
Le cycle biologique de l’ours polaire est intimement lié à la glace de mer, qui lui fournit une plateforme sur laquelle il peut chasser, voyager, s’accoupler et creuser sa tanière. Au printemps, les ours polaires s’attaquent surtout aux jeunes phoques annelés qui sont naïfs et qui constituent une source de nourriture très calorique. Cependant, les données récentes indiquent que les taux d’ovulation, et donc les taux de naissance, des phoques annelés pourraient être influencés par les variations à long terme du milieu marin arctique (Ferguson et coll. 2017), remettant ainsi en question le rôle que joue la glace de mer dans les interactions entre ces deux espèces.
En raison de la réduction de l’étendue de la glace de mer (Figure 2), les ours polaires passent maintenant plus de temps sur la terre ferme et ont commencé à utiliser d’autres ressources alimentaires. Cependant, l’évolution du cycle biologique et de la physiologie de l’ours polaire l’a amené à se nourrir de mammifères marins riches en lipides, de sorte que les ressources alimentaires terrestres, comme les œufs d’oiseaux de mer, ne lui permettront probablement pas de maintenir son état corporel dans un contexte marqué par la réduction à long terme de l’étendue de la glace de mer. Certaines données semblent indiquer, comme pour le phoque annelé, que l’ours blanc subit peut-être plus de stress en raison de la réduction à long terme de la disponibilité de ses proies (Environnement et Changement climatique Canada, données non publiées). On prévoit également que la réduction de l’étendue de la glace de mer augmentera le nombre d’interactions entre l’homme et l’ours polaire (Towns et coll. 2009), ce qui pourrait avoir une incidence sur la survie des individus. Que signifie tout cela pour les populations d’ours polaires?

Figure 2. (a) Arrivée précoce de la débâcle à long terme et (b) prolongation de la période sans glace dans l’ouest de la baie d’Hudson au Canada (source des données : Centre national de données sur la neige et la glace, https://nsidc.org/data/NSIDC-0192).
Description longue
Graphique A. Un diagramme de dispersion de la diminution à long terme de la date de débâcle dans l’ouest de la baie d’Hudson. La diminution a une valeur R2 de 0,3451. L’axe des abscisses (en bas) correspond aux années 1975 à 2017, et l’axe des ordonnées (latéral) correspond au jour ordinal de l’année de 130 à 200. Graphique B. Un diagramme de dispersion de l’augmentation à long terme de la durée de la période sans glace dans l’ouest de la baie d’Hudson, au Canada. L’augmentation a une valeur R2 de 0,4478. L’axe des abscisses (en bas) correspond aux années 1975 à 2017. L’axe des ordonnées (latéral) correspond au nombre de jours sans glace de 120 à 200.
En 2016, Lunn et coll.ont publié une analyse à long terme de la démographie de la population d’ours polaires dans l’ouest de la baie d’Hudson qui se penche sur la variation individuelle de la survie par rapport aux changements de la dynamique de la glace de mer. Ils ont constaté que la survie des ours femelles jeunes et adultes était liée à des changements dans la dynamique de la glace de mer qui ont influé sur la disponibilité et la qualité de l’habitat des ours blancs. En même temps, ils ont pu documenter une diminution de 30 % de la taille de la population d’ours polaires de l’ouest de la baie d’Hudson entre 1987 et 2011 (Figure 3). Des relevés aériens ultérieurs ont confirmé que la population a diminué pour atteindre environ 842 ours (Dyck et coll. 2017).

Figure 3. Le déclin à long terme de la taille de la population d’ours blancs de l’ouest de la baie d’Hudson de 1987 à 2011 s’explique par une réduction de la disponibilité de la glace de mer (source : Lunn et coll. 2016).
Description longue
Un graphique linéaire de la diminution à long terme de la taille de la population d’ours blancs de l’ouest de la baie d’Hudson de 1987 à 2011, qui s’explique par une réduction de la disponibilité de la glace de mer (source : Lunn et al. 2016). L’axe des abscisses (en bas) correspond aux années (1987 à 2011) et l’axe des ordonnées (latéral) correspond au nombre d’ours blancs, les données s’échelonnant entre environ 600 et 1400. Après 1986, une barre d’erreur est associée à chaque point de données. Les barres d’erreur indiquent un excédent ou un déficit de 10 à 15 %.
La relation mécaniste entre la dynamique de la glace de mer, l’état corporel des ours et, ultimement, la survie de l’ours blanc a été observée ailleurs. Des tendances à la baisse semblables en ce qui a trait à l’état corporel ont été observées initialement par Stirling et coll. (1999) dans l’ouest de la baie d’Hudson et ont maintenant été documentées dans le sud de la baie (Obbard et coll. 2016). Plus récemment, un relevé aérien a révélé un déclin d’environ 17 % de la population d’ours blancs du sud de la baie d’Hudson de 2011 à 2016 (Obbard et coll. 2018). Du point de vue énergétique, l’ensemble de ces données soulignent l’importance que revêt la glace de mer pour l’écologie alimentaire des ours polaires et les conséquences démographiques en aval qui peuvent résulter du déclin à long terme de l’état corporel. Des conséquences semblables chez les populations de proies (p. ex. déclin de l’état corporel du phoque annelé entraînant une réduction de la survie) pourraient avoir des effets en cascade sur la longévité à long terme des ours blancs dans toute leur aire de répartition.
Encadré : L’océan en fleur
Changements dans la phénologie du phytoplancton des plateaux aux bassins
Pierre Coupel, Christine Michel, Emmanuel Devred, Pêches et Océans Canada
Le moment des événements du cycle annuel (c.-à-d. la phénologie) influe sur le fonctionnement de l’écosystème marin dans son ensemble. Outre la floraison des algues de glace, la floraison printanière ou estivale du phytoplancton est souvent considérée comme l’événement le plus important du cycle saisonnier de production dans l’Arctique. Le transfert de la production primaire de la floraison phytoplanctonique de courte durée aux niveaux trophiques supérieurs dépend non seulement du couplage temporel et spatial entre le passage des brouteurs et le moment de la floraison, mais aussi de la composition taxonomique de la floraison. Dans un Arctique en plein réchauffement, le recul précoce de la glace de mer et l’englacement tardif modifient la phénologie, de la floraison phytoplanctonique. Les prévisions relatives à une deuxième prolifération automnale due à des saisons d’eaux libres plus longues (Kovacs et Michel 2011) sont maintenant documentées pour l’ensemble de l’Arctique et pour les plateaux canadiens (Ardyna et coll. 2014; Michel et coll. 2015).
La perte de glace pluriannuelle épaisse et l’amincissement général de la glace de mer de l’Arctique sont également à l’origine d’une augmentation marquée de la prévalence des conditions de lumière propices aux floraisons sous la glace. Au cours des dernières décennies, la fonte précoce et importante de la glace de mer a créé des conditions propices au développement de floraisons sous la glace, de sorte que près de 30 % de l’océan Arctique recouvert de glace est devenu un milieu favorable aux floraisons de phytoplanctons sous la glace en plein mois de juillet (Horvat et coll. 2017). L’une des conséquences importantes des floraisons sous la glace est qu’elles consomment une fraction substantielle des éléments nutritifs de surface au détriment de la production primaire dans la zone de glace marginale après le retrait de la glace (Palmer et coll. 2014). Bien que le rayonnement ultraviolet et les brouteurs de zooplancton aient peu d’effet sur la production primaire sous la glace, ils peuvent réduire l’ampleur de la production primaire en eaux libres, ce qui a d’importantes répercussions sur la production transférée aux réseaux trophiques pélagiques ou benthiques. La modification de la période de production primaire peut également avoir une incidence sur la productivité totale de l’écosystème en déséquilibrant la production dans la glace, en dessous de la glace et en eaux libres, et peut nuire aux transferts dans le réseau trophique en entraînant un décalage des cycles biologiques des brouteurs qui peut avoir des répercussions en cascade sur des niveaux trophiques supérieurs.
En plus de ces changements de saisonnalité, on observe également un déplacement de la lisière des glaces du plateau au bassin. Puisque l’emplacement de la lisière des glaces par rapport à la topographie est un paramètre clé de la remontée d’eau profonde et du mélange (Carmack et Chapman 2003), la connaissance de la distribution spatio-temporelle de la lisière des glaces est cruciale pour comprendre et prévoir les changements liés à l’ampleur et au type de producteurs primaires ainsi qu’aux réseaux trophiques qui en dépendent dans un Arctique en pleine évolution. Un schéma illustrant les changements liés à la phénologie de la production primaire sur les plateaux et les bassins, qui sont dus au réchauffement climatique, est présenté à la Figure 4 et décrit ci-dessous.
Sur les plateaux productifs de l’Arctique, la débâcle printanière déclenche habituellement une floraison courte et intense à la lisière des glaces. Cette floraison est dominée par de grandes diatomées, comme les espèces Chaetoceros et Thalassiosira, qui stockent l’énergie sous forme lipidique et sont très efficaces pour transférer cette énergie aux ressources exploitables, comparativement au phytoplancton de plus petite taille. Dans les régions encore couvertes de glace, la floraison d’algues de glace ou de phytoplancton sous la glace peut survenir lorsque suffisamment de lumière traverse la couverture glaciaire. À la suite de tels événements, la nature de la floraison estivale de phytoplancton change radicalement par rapport à la floraison qui se produit à la lisière des glaces. En réaction au manque d’éléments nutritifs à la surface, la floraison s’étend plus profondément dans la colonne d’eau où elle forme ce qu’on appelle un maximum de chlorophylle subsuperficiel. À mesure que les nutriments s’épuisent, de petites cellules phytoplanctoniques remplacent les diatomées, et les espèces adaptées à une faible luminosité, comme les espèces Micromonas sp., prennent le dessus lorsque le rayonnement solaire diminue et que l’hiver arrive.
Au cours des dernières années, des floraisons se sont formées à la lisière des glaces, au large des côtes. Bien que les floraisons hauturières soient dominées par les diatomées, l’ordre de grandeur de leur production est d’une fois inférieur à celui des floraisons qui se produisent sur le plateau en raison de la plus petite charge en éléments nutritifs de surface qui caractérise le bassin au départ (Coupel et coll. 2015). Simultanément, sur le plateau, le moment et l’emplacement des points chauds sont susceptibles de changer puisqu’ils dépendent de l’équilibre entre le mélange qui fournit les nutriments et la disponibilité de la lumière, qui sont tous deux liés à l’emplacement de la lisière des glaces. À la bordure du plateau, des conditions de vent favorables à la remontée d’eau profonde peuvent produire des floraisons automnales productives selon l’état de la glace et la lumière du jour.
Les différences régionales relatives au moment et à l’étendue de la superficie d’eaux libres ont d’importantes répercussions sur la phénologie des floraisons phytoplanctoniques (Barber et coll. 2015). Dans la mer de Barents, qui est influencée par l’Atlantique, les floraisons de phytoplancton commencent dès la fin avril alors qu’elles se développent habituellement après la mi-juin (Mundy et coll. 2014) ou la mi-juillet (Arrigo et coll. 2012) dans le secteur canadien. Dans l’ensemble, la dynamique complexe de la glace de mer influe sur le moment, l’emplacement, l’ampleur et la composition des producteurs primaires sur les plateaux et les bassins profonds de l’Arctique. Notre compréhension globale de la phénologie du phytoplancton par rapport à la dynamique des glaces est remise en question par les changements rapides qui sont en cours, et les effets de la cascade trophique ne sont toujours pas bien compris.

Figure 4. Événements annuels (changements phénologiques) de la production primaire de la glace de mer et de la colonne d’eau dans des conditions habituelles (panneau supérieur) et réduites (panneau inférieur) de couverture de glace sur les plateaux et dans les bassins de l’Arctique.
Description longue
Un infographique (bande dessinée) décrivant les événements annuels (changements phénologiques) de la production primaire de la glace de mer et de la colonne d’eau dans des conditions habituelles (panneau supérieur) et réduites (panneau inférieur) de couverture de glace sur les plateaux et bassins de l’Arctique.
Dans le panneau supérieur (scénario de couverture de glace typique), la glace de mer est plus épaisse et la débâcle a lieu à la fin de la période printanière/estivale. La glace de mer est davantage recouverte de neige. Le printemps, des algues de glace poussent au fond de la glace de mer. Les algues de glace se composent principalement d’espèces de diatomées pennées. Au moment de la débâcle au printemps-été, il y a une floraison courte et intense de phytoplancton à la lisière des glaces dominée par différentes espèces de diatomées de grande taille. Dans des conditions représentatives, la floraison à la lisière des glaces se produit généralement lorsque la glace se trouve sur le plateau continental. L’été, la zone de grands fonds connaît une floraison composée de petites espèces de phytoplancton.
Dans le panneau inférieur (scénario de couverture de glace réduite), la glace de mer est plus mince et moins recouverte de neige. La débâcle a lieu plus tôt dans la saison et la surface de la glace printanière/estivale comporte des zones de neige et de glace fondues, appelées mares de fonte. Une couche d’eau douce s’accumule à la surface durant la période de fonte des glaces. Les algues de glace continuent de pousser au fond de la glace le printemps et l’été et dans les eaux à bassin profond. Différentes espèces peuvent pousser, ce qui crée des tapis sous la glace qui pendent en longs brins. Une floraison de phytoplancton sous la glace, plus petite que celle de phytoplancton à la lisière des glaces dans des conditions représentatives, se développe. La floraison de petit phytoplancton dans les eaux du bassin est également moins importante que dans des conditions glacielles normales. Dans le scénario de glace réduite, il pourrait aussi y avoir un point chaud de floraison de phytoplancton au large et à l’automne, les vents pourraient brasser l’eau, créant des remontées d’eau qui apportent du nitrate (NO3) aux eaux de surface, où une floraison de phytoplancton automnale, qui passe des diatomées de grande taille à des diatomées de petite taille au fil du temps, peut se développer.
Encadré : Le phoque annelé et le déclin de la glace de mer
Épisode de chaleur extrême dans la baie d’Hudson et réponse du phoque annelé
Steve Ferguson, Pêches et Océans Canada

Figure 5. Phoque annelé sur la glace de mer (photo : relevé des phoques de la National Oceanic and Atmospheric Administration, domaine public, photo tirée de Wikimedia Commons).
’un des grands événements de l’histoire des changements climatiques est la perte de la glace de mer dans les régions polaires, et plus particulièrement la perte d’habitats essentiels pour les mammifères. Au cours des deux ou trois dernières décennies, les mammifères marins étudiés dans la mer de Beaufort ont réagi différemment aux changements liés à l’étendue et à la persistance de la glace de mer. L’état des jeunes baleines boréales (Balaena mysticetus) s’est amélioré avec le temps, tandis que celui des phoques annelés (Pusa hispida) et des bélugas (Delphinapterus leucas) s’est détérioré (Harwood et coll. 2015a). Toutefois, des questions subsistent quant aux causes réelles de ces réponses divergentes et à ce que ces réponses signifient pour une espèce ou un écosystème marin donné. Une étude récente menée dans l’Arctique canadien portait sur les changements démographiques (p. ex. perturbation de la reproduction, faible survie des petits, mortalité élevée) des populations de phoques annelés (Figure 5) liés aux facteurs de stress environnementaux.
La saisonnalité de la glace de mer est essentielle pour les phoques annelés. Ils ont besoin de glace de mer au printemps pour la mue, longue période où ils perdent leur fourrure et leur peau pour développer un nouveau pelage, ainsi que pour la reproduction. Pendant la saison estivale sans glace, ils se nourrissent en eaux libres et accumulent leurs réserves de graisse. Pendant l’hiver, ils donnent naissance et allaitent, mais sont désormais limités à de plus petites étendues de glace. Les phoques sont bien adaptés au caractère saisonnier de la glace de mer, mais la couverture de glace diminue en raison du réchauffement climatique. Ferguson et ses collaborateurs (2017) ont examiné les phoques annelés de la baie d’Hudson, l’une des régions les plus au sud de leur aire de répartition, ainsi que l’étendue de la glace de mer. La région traverse un cycle complet de perte et de reformation de la glace (Figure 6).

Figure 6. Concentration de glace de mer pour chaque jour de l’année de 2003 à 2013 dans la baie d’Hudson. Les différentes couleurs représentent les différentes années. La concentration de 50 % est indiquée par la ligne horizontale pointillée et est considérée comme le point de rupture de la débâcle (< 50 %) et du gel (> 50 %). Remarquez notamment les années indiquées en gris (la plus faible concentration de 2010 à gauche) et en mauve (la plus faible concentration de 2011 à droite) [source : Ferguson et coll. 2017].
Description longue
Graphique linéaire de la concentration de glace de mer chaque jour de l’année à partir de 2003-2013 dans la baie d’Hudson. Chaque année est représentée par une ligne de couleur différente. L’axe des abscisses (en bas) correspond au jour de l’année de 0 à 365. L’axe des ordonnées (latéral) correspond à la concentration de glace sur une échelle de 0 à 1. Il y a une ligne horizontale pointillée à une concentration des glaces à 0,5 ou à 50 %, ce qui est considéré comme le point de rupture de la débâcle (<50 %) et du gel (>50 %). Toutes les lignes avoisinent une concentration des glaces à 100 % autour du jour 50, puis déclinent à zéro sur une période d’environ 100 jours (p. ex. du jour 125 au jour 225), ce qui illustre que la baie d’Hudson est libre de glace l’été. Les valeurs des lignes augmentent après le jour 300. Il faut noter la ligne de l’année 2010 en gris, qui affiche la plus faible valeur du côté gauche du graphique (p. ex. débâcle hâtive), et la ligne de l’année 2011 en pourpre, qui affiche la plus faible concentration de glace du côté droit du graphique.
En analysant les données sur la glace de mer et le climat, il est apparu évident que la débacle se produit de plus en plus tôt et le gel de plus en plus tard dans la baie d’Hudson, ce qui indique que la saison des glaces est de plus en plus courte. Entre 1979 et 2014, il n’y a eu aucun lien entre les indices climatiques et les dates de la débâcle ou du gel. Cela signifie que le raccourcissement de la saison de glace de mer n’est pas lié aux régimes climatiques naturels, mais qu’il est vraisemblablement le résultat direct des changements climatiques d’origine humaine. La plus longue saison sans glace s’est produite en 2010, année où la débâcle est survenue en mai et où les eaux n’ont pas regelé avant janvier 2011 (Figure 6).

Figure 7. a) Taux annuel d’ovulation pour chaque année (notez le faible taux enregistré en 2011), b) Pourcentage annuel de petits dans le prélèvement (représentation du recrutement des petits; notez la récente tendance à la baisse), c) Relation entre l’état corporel du phoque et l’année (notez la baisse), d) Relation entre le niveau de cortisol (stress) et l’année (notez la hausse au fil du temps) [source : Ferguson et coll. 2017].
Description longue
La figure se compose de quatre graphiques liés aux phoques annelés dans la baie d’Hudson. Le graphique A (diagramme à barres) montre le taux d’ovulation en pourcentage (axe des ordonnées) des phoques annelés femelles pour les années 2003 à 2013. Il convient de souligner l’année faible sur le plan de l’ovulation, c’est-à-dire légèrement au-dessus de 50 %, en 2011. Les taux pour la période de 2007 à 2013 sont variables, et la majorité des barres se situent entre 75 et 100 %. Les données ne sont pas disponibles pour la période de 2004 à 2006. Le graphique B (diagramme à barres) montre le pourcentage de jeunes phoques annelés dans la récolte communautaire de 2003 à 2013. Les petits de la récolte sont utilisés à titre représentatif du recrutement des petits (survie d’un stade biologique au suivant). On note une tendance à la baisse pour la période de 2007 à 2013. Le graphique C (graphique linéaire) montre la relation entre l’état corporel du phoque annelé défini comme le pourcentage de graisse sur l’axe des ordonnées entre 2004 et 2014 sur l’axe des ordonnées. Une barre d’erreur est associée à chaque point de données et il y a un déclin général de l’état. Le graphique D (graphique linéaire) montre la relation entre le niveau de stress du phoque annelé mesuré par les concentrations de cortisol en nanogramme par gramme, pour les années 2003 à 2012. Une barre d’erreur est associée à chaque point de données et il y a une augmentation générale du stress au fil du temps.

Figure 8. Blanchon annelé (photo : Shawn Dahle, NOAA, Polar Ecosystems Program research cruise, domaine public, tiré de Wikimedia Commons).
En examinant l’état corporel, l’état de reproduction, le recrutement des petits et le niveau de stress de 1 425 phoques capturés dans le cadre de la chasse de subsistance des Inuits dans la baie d’Hudson entre 2003 et 2013, on a constaté que l’état corporel du phoque annelé est passé de 55 % de petit lard en 2004 à seulement 40 % en 2012, mais que cette proportion est remontée à 48 % en 2013. La détérioration de l’état corporel était liée au prolongement de la période sans couverture de la glace (saison de glace de mer plus courte). La concentration de cortisol (une mesure du stress) a augmenté avec le temps chez les phoques annelés. En 2010, les taux de cortisol étaient élevés et montraient une grande variabilité. Les taux d’ovulation ont été faibles l’année suivante (2011), ce qui est probablement attribuable au fait que les phoques annelés ont été soumis à un stress élevé en 2010 (Figure 7).
Que signifient ces changements et peut-on dresser un portrait d’ensemble de la situation? Cette étude montre que le déclin de l’état corporel du phoque annelé coïncide avec le déclin de la glace de mer, l’une des nombreuses conséquences des changements climatiques. L’étude établit en outre une relation entre l’événement climatique de 2010 et les changements démographiques liés aux populations de phoques annelés, car l’état corporel des individus s’est détérioré, les phoques ont été stressés et le taux d’ovulation des femelles a diminué, ce qui a entraîné une diminution du nombre de petits (Figure 8) dans les années suivantes. Cet événement climatique est lié à des régimes climatiques à grande échelle qui indiquent que les cycles à climat contrôlé continueront d’avoir une incidence sur l’état corporel et les caractéristiques démographiques des phoques. Dans la baie d’Hudson, l’état des phoques s’est quelque peu amélioré au cours des années suivant 2010. Toutefois, la cohorte de 2010 sera peu nombreuse en raison des conditions extrêmes observées cette année-là.
Par quel mécanisme la perte de glace de mer (ou d’autres facteurs) a-t-elle entraîné la détérioration de l’état corporel et l’augmentation du stress du phoque annelé? Le prolongement de la période sans couverture de la glace en 2010 pourrait avoir nui à l’accès des phoques annelés aux proies ainsi qu’à l’abondance et à la répartition des proies. L’élévation des températures de la mer vers la fin de l’automne pourrait avoir entraîné une hyperthermie chez les phoques gras et les phoques échoués sur les rives. Les phoques présentaient également des signes de léthargie anormale, ce qui peut indiquer la présence d’une maladie susceptible d’avoir été causée par l’interruption de la mue. La maladie a pu à son tour augmenter le risque de prédation par les ours polaires (Ursus maritimus) (Figure 9). On voit donc que le mécanisme qui est à l’origine de la détérioration de l’état corporel du phoque pendant les longues périodes sans couverture de la glace n’est pas encore bien compris.
Selon les modèles atmosphériques à long terme, des événements épisodiques comme celui de 2010 devraient se produire tous les 10 à 15 ans, mais de façon imprévisible. C’est la combinaison de la perte graduelle de glace de mer causée par les changements climatiques et de ces événements épisodiques imprévisibles qui est la plus susceptible d’avoir des répercussions majeures sur l’état corporel des phoques annelés et, à long terme, sur leur abondance et leur répartition.
Cette recherche fournit de plus amples renseignements sur ce que nous réserve l’avenir, mais il demeure difficile de faire des prévisions. D’autres recherches seront nécessaires pour déterminer quel est le mécanisme à l’origine du déclin de l’état corporel entraîné par la perte de la glace de mer, comment les populations de phoques s’adapteront aux changements climatiques et comment les écosystèmes plus vastes seront touchés à leur tour.

Figure 9. Ours polaire mangeant un phoque capturé sur le rivage au nord de Churchill, en octobre 2010, pendant l’année inhabituelle où des phoques annelés sont sortis de l’eau et se sont aventurés près des ours polaires en attendant le retour de la glace de mer (photo : Daryl Hedman).
Description longue
Photographie d’un ours blanc sur un rivage rocheux près de Churchill, au Manitoba. Les pattes avant de l’ours blanc sont tachées de sang, et il tient dans sa gueule les restes de sa proie de prédilection, un phoque annelé. L’ours a attrapé le phoque sur la terre ferme durant l’année 2010, où il n’y a pas eu beaucoup de glace de mer et où les phoques sont sortis hors de l’eau près des ours blancs en attendant le retour de la glace de mer.
Encadré : Une année différente
Variabilité de l’écosystème dans le sud de la mer de Beaufort au Canada
Andrew Majewski, Andrea Niemi, Jane Eert, Christine Michel, Ellen Lea, Lisa Loseto, Jim Reist, Pêches et Océans Canada
Maxime Geoffroy, Université Memorial
Au cours des 15 dernières années, l’écosystème marin de la mer de Beaufort a suscité l’attention de nombreux chercheurs. La recherche administrée par le gouvernement fédéral, y compris le Programme d’études du milieu marin côtier du Nord (MPO 2003-2009), ArcticNet (2003 à ce jour), l’évaluation environnementale régionale de la mer de Beaufort (2011-2015) et l’évaluation actuelle des écosystèmes marins de la mer de Beaufort au Canada (EEM-MBC 2017), ont permis de générer des données biologiques de référence pour le milieu marin hauturier et commencent, pour la première fois, à produire une série chronologique de données biologiques associées aux caractéristiques physiques et chimiques des habitats. Les résultats indiquent une variabilité spatiale et interannuelle importante pour plusieurs composantes clés de l’écosystème, posant ainsi un défi lié à la détermination de la variabilité naturelle dans un environnement qui évolue lui aussi rapidement en raison des changements climatiques. Ce défi touche également d’autres régions de l’Arctique canadien parmi lesquelles plusieurs sont peu étudiées.

Figure 10. Biomasse mésopélagique de la morue polaire dans le sud de la mer de Beaufort canadienne calculée à partir de données hydroacoustiques (source : M. Geoffroy, données non publiées).
Description longue
Diagramme à barres de la biomasse mésopélagique de la morue arctique sur l’axe des ordonnées (latéral), qui varie de 0 à 2,5 grammes par mètre carré, et des années 2010 à 2014 sur l’axe des abscisses (en bas). Une barre d’erreur est associée à chaque barre. Les valeurs de la biomasse ont été calculées à partir des données hydroacoustiques. Les données indiquent une variabilité élevée entre les années caractérisées par une très faible biomasse, par exemple moins de 0,1 gramme par mètre carré en 2014. Les valeurs moyennes de la biomasse pour 2010 et 2012 se chiffrent entre 1 et 1,5 gramme par mètre carré, et les valeurs moyennes de la biomasse varient entre 0,5 et 0,75 gramme par mètre carré.
La morue polaire (Boreogadus saida) est un élément important de la base fourragère marine de la mer de Beaufort et joue un rôle important à la fois comme brouteur et comme proie des poissons, des phoques, des baleines et des oiseaux (Mueter et coll. 2016). Des relevés hydroacoustiques conjoints effectués à bord du navire de la Garde côtière canadienne Amundsen et du F/V Frosti entre 2010 et 2014 ont révélé une variabilité interannuelle importante de la biomasse de la morue polaire, tant pour les spécimens de moins d’un an (âge 0) que pour les spécimens adultes, et une forte diminution de la biomasse des morues adultes a été observée au cours de l’année d’échantillonnage 2014 (Figure 1 0). Ce déclin a été précédé d’une baisse générale de l’abondance et de la biomasse de la morue d’âge 0 entre 2010 et 2013. Dans une analyse ultérieure, ces données ont été intégrées à des ensembles de données acoustiques provenant de l’ensemble de l’Arctique canadien et ont permis de déterminer que la biomasse de la morue d’âge 0 en août et en septembre était corrélée négativement à la semaine de débâcle et positivement à la température à la surface de la mer (Bouchard et coll. 2017), ce qui indique un contrôle ascendant pour certains niveaux trophiques, comme les poissons pélagiques.

Figure 11. Béluga ayant la bouche pleine de lançons (photo gracieusement fournie par Loseto et coll.2018a).
arallèlement à la faible biomasse de la morue polaire adulte dans la mer de Beaufort canadienne en 2014, des observations remarquables ont été faites dans d’autres secteurs de l’écosystème, y compris en régions côtières. Plus de 30 bélugas ont été capturés près d’Ulukhaktok, seul prélèvement de cette ampleur jamais enregistré pour cette communauté (Loseto et coll. 2018a). Les observations effectuées dans l’estuaire du Mackenzie et dans la baie Darnley dans le cadre des programmes de surveillance écologique indiquent que l’estomac des bélugas était généralement vide au moment du prélèvement (Harwood et coll. 2015b). Le régime alimentaire des bélugas de l’est de la mer de Beaufort a été principalement déduit d’études sur les biotraceurs (Loseto et coll. 2009), d’études sur l’utilisation de l’habitat menées pendant les expériences de marquage (Hauser et coll. 2017) et de relevés aériens (Hornby et coll. 2016, 2017). Toutes ces études montrent que la morue polaire est l’une des proies principales du béluga dans les eaux marines hauturières. Les bélugas capturés à Ulukhaktok en 2014 étaient les seuls à avoir de nombreuses proies dans leur estomac, mais ne semblaient pas se nourrir de morue polaire de façon substantielle. C’est plutôt le lançon (espèces Ammodytes) (Figure 11) qui était la proie dominante observée dans les entrailles, avec le calmar (déduit par la présence de becs) et d’autres espèces de poissons dans une bien moindre mesure (Loseto et coll. 2018). Les bélugas capturés dans la région désignée des Inuvialuit en 2014 avaient un indice d’état corporel inférieur à celui des individus observés au cours des trois saisons précédentes, ce qui donne à penser que la variabilité annuelle des proies pourrait être associée à une variation interannuelle de l’état des bélugas (Choy et coll. 2017).
Les contenus intestinaux de l’omble chevalier (Salvelinus alpinus) prélevés à Ulukhaktok en 2014 et en 2015 indiquent que le régime alimentaire de l’espèce peut être très variable et peut être lié à la disponibilité des proies préférées. Comme pour le béluga, le lançon était très répandu dans le régime alimentaire de l’omble chevalier, tout comme les amphipodes marins. Ces résultats contrastent avec les échantillons recueillis à Ulukhaktok en 1977 et en 1978, qui contenaient surtout de la morue polaire (E. Lea, données non publiées).
Les estimations de la production primaire sont aussi un indicateur de la variabilité interannuelle apparente de l’écosystème de la mer de Beaufort. Malgré une année de biomasse apparemment faible pour la morue polaire en 2014, et malgré des changements simultanés dans la distribution et le régime alimentaire des espèces de subsistance, la biomasse des producteurs primaires, qui est indiquée par les concentrations de chlorophylle a, a atteint des valeurs six fois plus élevées qu’en 2013 ou en 2017, l’accumulation de biomasse étant la plus élevée dans le sud-ouest de l’île Banks (C. Michel, données non publiées) (Figure 12). Ces résultats indiquent que des ressources suffisantes étaient disponibles, du moins à l’échelle locale, pour soutenir une forte productivité secondaire.
Les observations et les résultats tirés de la saison des eaux libres de 2014 fournissent un exemple distinct de la variabilité interannuelle qui s’est produite à de multiples niveaux trophiques et qui a été observée tant au large qu’en milieu côtier. La variabilité influe sur les récoltes de subsistance de la région, entraînant ainsi des avantages et des incertitudes pour différentes collectivités (Loseto et coll. 2018a). Compte tenu du nombre limité d’années où des observations soutenues ont été effectuées dans l’écosystème de la mer de Beaufort canadienne, il n’est pas possible de désigner l’année 2014 à titre d’anomalie écologique. D’autres travaux sont nécessaires pour comprendre les facteurs des changements observés dans les écosystèmes même si l’on reconnaît que ces facteurs peuvent être à l’origine des changements survenus au cours des saisons ou des années précédant la saison des eaux libres de 2014. On s’attend à ce que la variabilité et la survenance d’événements anormaux deviennent plus fréquentes à mesure que la planète se réchauffe (Groupe d’experts intergouvernemental sur l’évolution du climat, 2014). Par conséquent, la surveillance écologique nécessaire pour comprendre les facteurs de variabilité de l’écosystème, y compris les couplages physiques et biologiques, est essentielle pour prévoir les effets locaux et en aval des changements climatiques dans la mer de Beaufort, ainsi que pour orienter les stratégies d’adaptation dans la région désignée des Inuvialuit (RDI).

Figure 12. Concentrations intégrées de chlorophylle a dans la mer de Beaufort pour la zone euphotique, en 2013, 2014 et 2017 (source : C. Michel, données non publiées, cartes créées avec Ocean Data View, Schlitzer, R., https://odv.awi.de, 2018).
Description longue
Trois graphiques cartographiques qui incluent les zones marines de la mer de Beaufort (au large des côtes), du plateau du Mackenzie et du golfe Amundsen sont montrés. Le continent des Territoires du Nord-Ouest se trouve le long du bas de chaque carte et de la partie sud de l’île Banks et du côté est avoisinant de l’île Victoria se trouve le long du côté supérieur droit. Les emplacements des stations d’échantillonnage sont représentés par des points noirs pour les années 2017 (en haut), 2014 (au milieu) et 2013 (en bas). À chaque station, les concentrations de chlorophylle a ont été mesurées et intégrées pour la zone euphotique. Les concentrations de chlorophylle a sont présentées comme un graphique de couleur de la surface. Les zones rouges et jaunes indiquent des concentrations plus élevées, alors que les tons de pourpre et de bleu représentent de faibles concentrations. Les concentrations de chlorophylle a intégrées, en mg par mètre carré, variaient de près de 0 à environ 25, 200 et 30, en 2013, 2014 et 2017, respectivement. En 2014, la chlorophylle a atteint des valeurs six fois supérieures à celles de 2013 ou de 2017. Les concentrations des trois années ont été les plus élevées dans le golfe Amundsen, la plus forte accumulation de biomasse ayant été enregistrée dans le sud-ouest de l’île Banks en 2014 et en 2017.
Encadré : Sanctuaire de l’Arctique
Les eaux du Nord – Sanctuaire de forte productivité et la biodiversité qui y est associée
Cortney Watt et Christine Michel, Pêches et Océans Canada
Pendant la période de couverture de la glace, les polynies fournissent des zones fiables d’eaux libres où les mammifères marins et les oiseaux se rassemblent. Les eaux du Nord de la baie de Baffin, entre le Groenland et le Canada, constituent la polynie la plus vaste et la mieux caractérisée de l’Arctique canadien. La polynie doit son existence à un pont de glace qui se forme habituellement dans le détroit de Nares et qui retient la glace dérivant de l’océan Arctique, ainsi qu’à une combinaison de processus thermiques qui reposent sur l’arrivée d’une chaleur latente (poussée par le vent) et sensible (réchauffement des océans).
Avant que s’opèrent les changements rapides qui ont touché la glace de mer dans l’Arctique au cours des deux dernières décennies, les eaux du Nord, aussi appelées Pikialasorsuaq, étaient considérées comme l’une des régions les plus productives de l’Arctique (Deming et coll. 2002). Pikialasorsuaq abrite de grandes populations d’oiseaux de mer et de mammifères marins (Heide- Jørgensen et coll. 2013b), et l’établissement humain sur les côtes adjacentes remonte à 4 500 ans avant notre ère (Jeppesen et coll. 2018), ce qui démontre l’importance et la fiabilité de ce secteur. Quatorze espèces d’oiseaux de mer utilisent régulièrement la polynie pour la reproduction et le Mergule nain, (Alle alle), est l’espèce la plus abondante avec plus de 30 millions de couples nicheurs (Egeyang et coll. 2003; Davidson et coll. 2018). Des colonies reproductrices de centaines de milliers de marmettes de Brünnich (Uria lomvia) et de dizaines de milliers d’eiders à duvet (Somateria molissima) sont également présentes dans la région (Burnhan et coll. 2012; Merkel et coll. 2014). Les mammifères marins dépendent également de cette polynie puisqu’elle est pour eux un refuge contre la couverture de glace et un accès à l’air. Le narval (Monodon monoceros), le béluga (Delphinapterus leucas) et la baleine boréale (Balaena mysticetus) sont des espèces qui fréquentent régulièrement les polynies et les chenaux pendant l’hiver. En 2009 et en 2010, on estimait à plus de 27 000 le nombre de mammifères marins habitant les eaux du Nord au mois de mai, parmi lesquels on comptait des bélugas, des narvals, des morses (Odobenus rosmarus), des phoques annelés (Pusa hispida), des phoques barbus (Erignathus barbatus) et des ours polaires (Heide-Jørgensen et coll. 2013). En avril 2014, plus de 13 500 morses, bélugas, narvals et phoques barbus ont été observés dans la région (Heide-Jørgensen et coll. 2016). Les mammifères marins et les oiseaux de mer dépendent également d’autres polynies de l’Arctique canadien situées dans le sud de la baie de Baffin, le détroit d’Hudson et la baie de Cumberland (Lewis et coll. 2009; Watt et coll. 2016, 2017; Chambault et coll. 2018).
Le dégel précoce des eaux du Nord permet le développement d’une floraison de phytoplancton plusieurs mois plus tôt que dans les eaux voisines couvertes de glace de l’archipel canadien (Tremblay et coll. 2006a; Michel et coll. 2015). Des transferts efficaces vers l’écosystème pélagique (Tremblay et coll. 2006b) soutiennent le réseau trophique marine productive. Une récente analyse chronologique des estimations par télédétection de la biomasse de phytoplancton dans les eaux du Nord au cours des deux dernières décennies (de 1998 à 2014) montre une baisse importante de l’ampleur de la floraison malgré la variabilité interannuelle de la série d’observations (Marchese et coll. 2017). La grande variabilité interannuelle est attribuable à un équilibre fragile entre les forçages océanographiques et climatiques, qui donne lieu à des floraisons plus longues et plus courtes lors des années où la couverture de glace est plus mince ou plus épaisse, respectivement. Le déclin récent de la biomasse et de la production de phytoplancton est également documenté par des mesures in situ (Blaiset coll. 2017) (Figure 13) il est attribué à l’évolution des conditions de glace de mer et au retard ou à l’absence de formation du pont de glace dans le détroit de Nares.
Ensemble, ces résultats indiquent que Pikialasorsuaq, une région connue depuis longtemps pour sa productivité élevée, récurrente et prévisible et son abondance de ressources marines, a subi les effets néfastes des changements climatiques au cours de la dernière décennie. En prévision des changements futurs, la Commission Pikialasorsuaq (pikialasorsuaq.org) coordonne les efforts déployés au Nunavut et dans le nord du Groenland pour protéger, surveiller et gérer la santé de la polynie Pikialasorsuaq pour les générations futures. En 2017, la Commission a demandé la création d’une aire protégée délimitée et gérée par les Inuits dans la zone d’importance écologique et culturelle des eaux du Nord (Commission Pikialasorsuaq 2017). Un cadre de mise en œuvre des options de gestion a été établi en 2018.

Figure 13. Série chronologique de la biomasse (a) et de la production primaire (b) de chlorophylle a fractionnée par taille de 1999 à 2011, à l’automne, dans la baie de Baffin. Les données ont été intégrées aux données sur la zone euphotique (jusqu’à 0,2 % d’irradiance en surface). En 1999, seules deux fractions de taille ont été mesurées. Les valeurs ont une moyenne de ± 0,5 au sud-est. Le graphique B indique que la production des grandes cellules a été de 3,2 mg C m -2 j-1 à l’automne 2011 (source : Blais et coll. 2017).
Description longue
Deux diagrammes à barres liés aux producteurs primaires durant l’automne dans la baie de Baffin. Le graphique A montre la biomasse moyenne de la chlorophylle a fractionnée par taille (écart-type de ± 0,5) sur l’axe des ordonnées (latéral), qui varie de 0 à environ 100 milligrammes par mètre carré pour les années 1999, 2006, 2007, 2008, 2010 et 2011 (axe des abscisses en bas). Pour 1999, deux fractions de taille de phytoplancton sont présentées comme différentes parties ombragées de la barre : 0,7-5 micromètres et plus de 5 micromètres. Pour les six autres années, trois fractions de taille sont indiquées : 0.7-5, 5-20 et plus de 20 micromètres. On observe une tendance à la baisse dans la chlorophylle a totale au fil des ans. Les tendances dans les classes de tailles ne sont pas expliquées dans le texte.
Le graphique B montre la production primaire moyenne fractionnée par taille (écart-type de ± 0,5), qui varie de zéro à environ 700 milligrammes de carbone par mètre carré par jour, pour les mêmes années que dans le graphique A. Les barres comprennent des zones ombragées foncées et claires afin de représenter la production primaire attribuée à deux fractions de taille de phytoplancton (0.7-5 et >5 µm). On observe une tendance à la baisse dans la production primaire totale au fil des ans. Les tendances dans les classes de tailles ne sont pas expliquées dans le texte.
Encadré : Extension des aires de répartition
Extension des aires de répartition et présence de nouvelles espèces
Karen Dunmall et Cory Matthews, Pêches et Océans Canada

Figure 14. Charlie Erigaktoak et Danny Gordon Jr. avec un saumon qu’ils ont pêché en 2016 à Shingle Point, au Yukon (photo : Michelle Gruben).
L’Arctique est de toute évidence une région isolée, intrinsèquement dynamique et extrêmement vaste, et certaines régions connaissent des changements rapides à l’égard de leur biodiversité qui ont des répercussions à la fois locales et mondiales. En effet, les changements climatiques sont actuellement la menace la plus importante pour la biodiversité de l’Arctique (CAFF 2013), car le Nord est perçu à la fois comme un havre de conservation mondial pour les espèces qui se déplacent vers le Nord (Yoon et coll. 2015) et comme un danger potentiel pour la conservation mondiale des espèces adaptées au froid dans un environnement en plein réchauffement (Reist et coll. 2006a). L’importance de l’évaluation de la biodiversité est ancrée dans la conciliation du potentiel émergent de l’Arctique avec la protection de son environnement, de ses espèces et de ses cultures autochtones.
Les espèces indicatrices pertinentes sur les plans biologique, culturel et économique fournissent de l’information pour évaluer les répercussions sur l’écosystème des changements environnementaux en cours dans l’Arctique. Ils servent également de guide pour la création de nouvelles possibilités. Toutefois, pour être un indicateur efficace de l’évolution de l’Arctique, les espèces doivent être sensibles aux changements environnementaux et refléter un changement survenu dans un laps de temps défini, détectable dans l’ensemble d’une région éloignée et supérieur à la variabilité ambiante, scientifiquement fondé, mais qui ne provient pas nécessairement de la science, et ayant un rapport direct avec des enjeux plus vastes (MPO 2015).
Le saumon du Pacifique (espèces Oncorhynchus) est un bon indicateur de changement parce qu’il a été désigné comme indicateur de l’état de l’océan (Irvine et Riddell 2007), qu’il réagit aux conditions environnementales changeantes (Grebmeier et coll. 2006; Dunmall et coll. 2013; Nielsen et coll. 2013), et qu’il peut être surveillé aux limites de son aire de répartition du Nord dans le cadre d’un programme de surveillance écologique par les collectivités (Dunmall et coll. 2013) (Figures 14 et 15). La répartition des espèces de saumon peut refléter l’évolution des conditions environnementales à la fois directement parce que les poissons, en tant qu’ectothermes, maintiennent leurs préférences thermiques par des choix comportementaux (Reist et coll.2006a), mais aussi indirectement en raison du lien qui existe entre une productivité accrue et la disponibilité des proies pour les espèces potentiellement colonisantes (Dunmall et coll. 2013). Bien que la présence du saumon en Arctique ne soit pas une nouveauté (examiné dans Nielsen et coll. 2013), les augmentations actuelles de l’abondance et de la répartition du saumon dans cette région reflètent probablement des changements à plus grande échelle. Le saumon est un indicateur unique des liens entre les océans, les pays, les cultures, les économies et les écosystèmes.
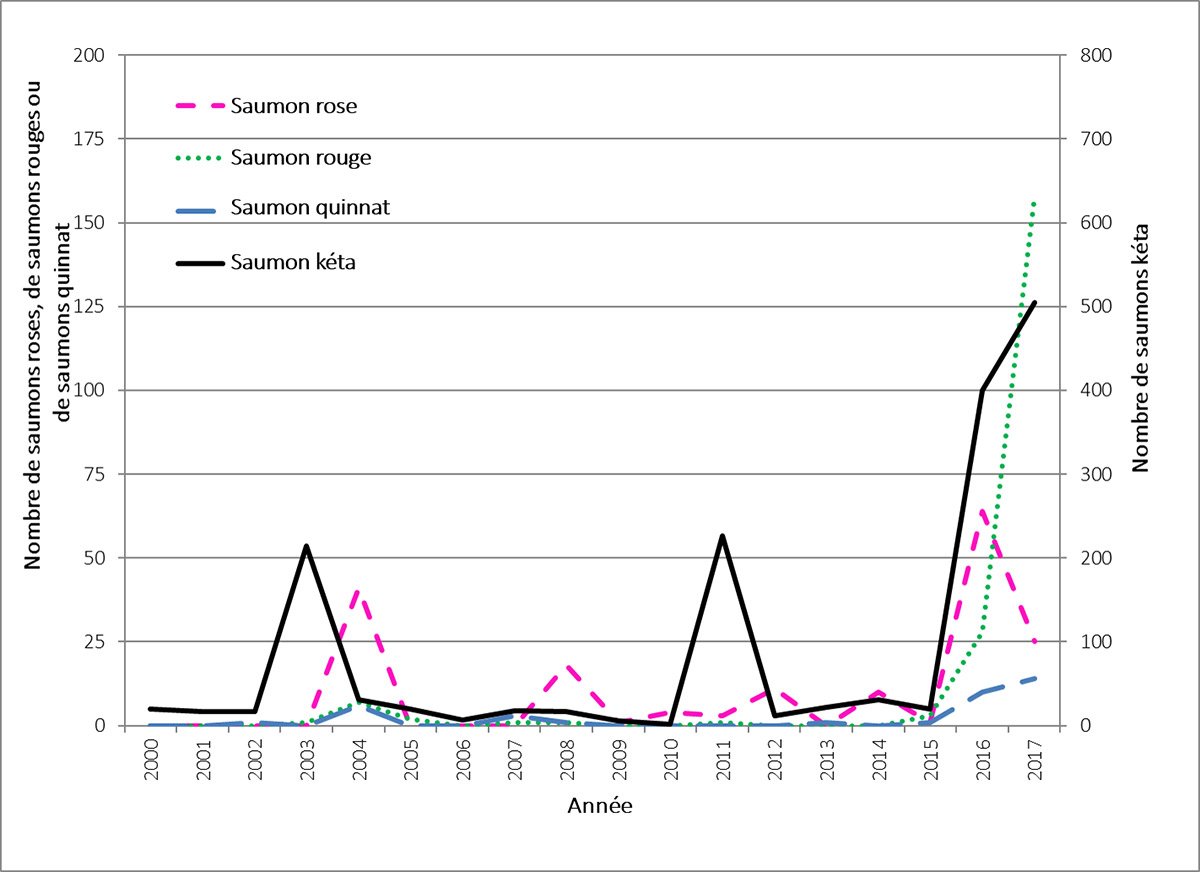
Figure 15. Nombre d’individus de chaque espèce de saumon du Pacifique transmis au programme de surveillance écologique par les collectivités du saumon de l’Arctique par les pêcheurs de l’ensemble de l’Arctique canadien de 2000 à 2017. Un seul saumon coho a été signalé au cours de cette période (en 2011); il n’est donc pas inclus dans le graphique (source : modifié de Dunmall et coll. 2018).
Description longue
Graphique linéaire du nombre de chaque espèce de saumon du Pacifique (axe des ordonnées latéral) transmis au programme de surveillance communautaire du saumon de l’Arctique par les pêcheurs de l’ensemble de l’Arctique canadien de 2000 à 2017 (axe des abscisses en bas). Le nombre de saumons roses, de saumons rouges et de saumons quinnat varie de quasi zéro à un peu plus de 150 individus. Le nombre de saumons kéta varie de quasi zéro à près de 500 individus. Le nombre de saumons kéta se situe autour de 25 pour la plupart des années et a augmenté à juste un peu plus de 200 individus en 2003 et en 2011 pour ensuite augmenter considérablement en 2016 (environ 395 individus) et en 2017 (500 individus). On dénombre moins de cinq saumons roses la plupart des années, sauf pour un sommet d’environ 35 individus en 2004 et un sommet légèrement plus élevé en 2016. Le nombre de saumons quinnat est également inférieur à cinq la plupart des années, mais a augmenté à 10 à 15 individus en 2016 et en 2017. Le saumon rouge affiche une très forte augmentation, passant à 150 individus en 2017. Toutes les espèces ont enregistré un déclin en 2018 par rapport à 2017. Un seul saumon coho a été signalé au cours de cette période (en 2011); il n’est pas inclus dans le graphique.
Les épaulards (Orcinus orca) représentent également la connectivité entre les océans du Canada et les changements qui s’y produisent. Dans l’est de l’Arctique canadien, les épaulards (Figure 16) sont présents de façon saisonnière de juillet à octobre environ, lorsque les eaux libres leur permettent d’entrer dans les baies et les bras de mer pour chasser divers mammifères marins. Les observations d’épaulards ont augmenté au cours des dernières décennies dans toute leur aire de répartition, soit du nord de l’île de Baffin au sud de la baie d’Hudson (Higdon et Ferguson 2009; Higdon et coll. 2013). Bien que les épaulards soient répartis dans le monde entier et qu’ils soient présents en densités relativement hautes à des latitudes élevées, ils évitent généralement les régions glacielles de l’Arctique (Matthews et coll. 2011). L’augmentation récente des observations a été corrélée à des réductions simultanées de l’étendue et de la persistance de la glace de mer à des endroits où des zones auparavant couvertes de glace qui constituaient des obstacles s’ouvrent maintenant et permettent le passage des épaulards dans des zones où ils ont rarement, voire jamais été observés (Higdon et Ferguson 2009). Les Inuits de l’est de l’Arctique canadien ont signalé que la présence d’épaulards augmente dans toute la région (Higdon et coll. 2013). La baie d’Hudson, en particulier, a connu une augmentation presque exponentielle du nombre d’observations d’épaulards au cours des dernières décennies, alors que la région a connu des réductions radicales de l’étendue des glaces marines (Higdon et Ferguson 2009). Bien que les données sur les observations, qui ne sont pas recueillies lors d’enquêtes organisées, soient susceptibles d’être faussées en raison d’une sensibilisation accrue au signalement, il semble probable que la hausse du nombre d’observations reflète un changement de répartition, un nombre plus élevé d’individus ou une combinaison des deux.
Les conséquences de l’accroissement de la présence des épaulards et de la diminution de la glace de mer de l’Arctique ont fait l’objet de recherches à Pêches et Océans Canada (MPO) au cours de la dernière décennie. Les connaissances écologiques inuites et les rapports d’observations historiques qui portent sur des événements de prédation indiquent que les mammifères marins sont les principales proies, sinon les seules, des épaulards de l’Arctique (Higdon et coll. 2013; Westdal et coll. 2016a). Les exercices de modélisation indiquent que la mortalité due à la prédation des épaulards pourrait être suffisamment élevée pour avoir une incidence sur d’autres populations de mammifères marins de l’Arctique (Ferguson et coll. 2012). D’autres études récentes menées par le MPO montrent que les effets négatifs de la prédation des épaulards vont au-delà de la mortalité directe des proies. Les épaulards, par exemple, ont une incidence importante sur le comportement et la distribution des narvals. En l’absence d’épaulards, les narvals préfèrent vivre en eaux libres et profondes, alors qu’en leur présence, ils préfèrent les zones littorales peu profondes (Breed et coll. 2017). Bien que ce comportement soit connu depuis longtemps des Inuits, cette étude est unique parce qu’elle montre que la réaction du narval est maintenue tant et aussi longtemps qu’il partage le bras de mer relativement grand avec les épaulards, et qu’elle persiste au-delà d’événements ponctuels de prédation. Le comportement de la baleine boréale (Balaena mysticetus) et le choix de l’habitat de la glace de mer sont également grandement influencés par la présence des épaulards. Les baleines boréales du golfe de Boothia préfèrent également un habitat en eaux libres en l’absence d’épaulards, mais elles se retirent rapidement sous la couverture de glace et près des rives en présence de tels prédateurs (C. Matthews, données non publiées). Encore une fois, le comportement a été observé à l’échelle du golfe pour toutes les baleines boréales marquées pendant toute la durée de leur présence. Cette réaction n’avait jamais été documentée à si grande échelle pour des vertébrés marins. Les changements prononcés liés au comportement et à l’utilisation de l’habitat des proies des mammifères marins de l’Arctique, qui sont entraînés par la présence des épaulards, pourraient se traduire par des effets coûteux non liés à la prédation, comme la perte de possibilités alimentaires ou un stress accru. Ces changements pourraient avoir un effet néfaste sur les populations de proies, et ces répercussions sont susceptibles d’être exacerbées par les changements climatiques (Breed et coll. 2017; C. Matthews, données non publiées).

Figure 16. Épaulard dans le détroit d’Éclipse, au Nunavut, à l’été 2018 (photo : Maha Ghazal).
Description longue
Photographie d’un épaulard nageant dans le détroit d’Eclipse au Nunavut à l’été 2018. On peut apercevoir des montagnes enneigées en arrière-plan. La grande nageoire dorsale est hors de l’eau et le souffle de la baleine est visible dans le ciel.
’extension prévue de l’aire de répartition des épaulards dans l’Arctique, cependant, n’est peut‑être pas sans équivoque. Certes, les observations d’épaulards ont augmenté dans l’est de l’Arctique canadien, mais le nombre d’emprisonnements d’épaulards dans les glaces s’est lui aussi accru. Hidgon et Ferguson (2014) et Westdal et coll.(2016b) font état de plusieurs emprisonnements mortels d’épaulards dans l’est de l’Arctique canadien depuis le début des années 1950, ce qui est plus que le nombre d’événements semblables déclarés au cours du siècle dernier. Au cours du plus récent de ces événements, en 2016, on a observé des épaulards hivernant dans le sud-est de la baie d’Hudson, mais on les a retrouvés morts le printemps suivant. Matthews et coll.(2019) ont émis l’hypothèse selon laquelle les baleines seraient entrées dans la baie d’Hudson à la poursuite des bélugas l’été précédent, mais n’auraient pas réussi à en sortir avant la formation des glaces et seraient mortes de faim après avoir été incapables de satisfaire leurs besoins énergétiques pendant l’hiver. Les quatre décès confirmés à la suite de l’événement le plus récent, combinés aux décès causés par les précédents emprisonnements dans les glaces, représentent une portion importante de la population estimée d’épaulards dans l’est de l’Arctique canadien (Young et coll. 2011). L’emprisonnement de l’épaulard dans les glaces est presque toujours mortel, et peut anéantir des groupes familiaux entiers et avoir des incidences démographiques à long terme (Higdon et coll. 2013). L’emprisonnement dans les glaces pourrait donc ralentir l’expansion de l’aire de répartition des épaulards de l’Arctique, notamment dans les régions où les épaulards qui ne sont pas habitués à la configuration de la glace de mer ne parviennent pas à sortir avant la formation des glaces en hiver (Matthews et coll. 2019).
Encadré : Points chauds de l’Arctique
Points chauds des mammifères marins : points focaux de transfert énergétique dans l’Arctique canadien
Dave Yurkowski, Pêches et Océans Canada
La quantification des attributs biogéographiques, comme les déplacements des prédateurs marins de l’Arctique et leur répartition, a d’importantes répercussions sur notre compréhension de la structure et du fonctionnement de l’écosystème arctique (Moore et Huntington 2008). Les prédateurs marins très mobiles (p. ex. les mammifères marins, les oiseaux de mer et les gros poissons) intègrent des ressources à de nombreuses échelles spatiales et temporelles et peuvent donc servir de sentinelles pour les zones à productivité élevée et les changements saisonniers dans des environnements très dynamiques comme l’Arctique (Boyce et coll. 2015). Il est difficile d’observer les animaux dans l’environnement dynamique du milieu marin arctique, mais l’utilisation de dispositifs de télémétrie animale a révolutionné notre compréhension de l’écologie du mouvement des espèces marines (Hussey et coll. 2015). Traditionnellement, les études de télémétrie sur les prédateurs marins de l’Arctique se sont concentrées sur une seule espèce ou quelques espèces, mais étant donné la quantité de données de télémétrie actuellement disponibles pour les prédateurs marins de l’Arctique, on peut maintenant quantifier les points chauds liées à la diversité des espèces et déduire l’emplacement des zones d’importance biologique supérieure (c.-à-d. des points chauds) pendant la période été-automne et hiver-printemps.
Une compilation des données existantes sur le suivi des animaux a été recueillie entre 1989 et 2016 pour 1 283 individus de 21 espèces marines arctiques emblématiques comprenant des cétacés, des pinnipèdes, des oiseaux de mer, des ours polaires (Ursus maritimus) et des poissons. Parmi les espèces emblématiques, on compte les bélugas (Delphinapterus leucas), les narvals (Monodon monoceros), les phoques annelés (Pusa hispida), les morses de l’Atlantique (Odobenus rosmarus rosmarus), les eiders à duvet (Somateria mollissima), les fulmars boréaux (Fulmarus glacialis), les marmettes de Brünnich (Uria lomvia) et les requins du Groenland (Somniosus microcephalus). Les points chauds se trouvaient généralement le long du plateau continental et du talus continental tout au long de l’été et de l’automne et se situaient généralement au large des zones connues de banquise en mouvement pendant l’hiver et le printemps, ce qui correspond généralement aux modèles de productivité saisonnière (Figures 17 et 18). Ces déplacements présentent une connectivité saisonnière et une connectivité entre les chenaux d’énergie hauturiers et littoraux pendant la période hiver-printemps et été-automne, respectivement. Plus précisément, à l’ouest, les eaux riches en nutriments de l’océan Pacifique et de la mer de Béring s’écoulent vers le nord à travers le détroit de Béring et le sud de la mer des Tchouktches, ce qui accroît la biomasse faunique pélagique et benthique dans la région et le long du plateau continental et du méridien vers le Delta du Mackenzie (Grebmeier et coll. 2006). Au cours de l’hiver et du printemps, des points chauds ont été observées dans les zones situées à l’ouest de la polynie du cap Bathurst. Dans l’Est, l’île de Baffin se compose de nombreux fjords productifs en raison de l’augmentation de la teneur en carbone organique de la colonne d’eau (Syvitski et coll. 1990). Pendant l’hiver, les points chauds liées à la diversité des espèces étaient concentrées dans les zones de banquise mobile dense de la baie de Baffin et du détroit de Davis. Dans le Sud, les points chauds liées à la diversité des espèces coïncidaient avec les modèles de productivité du complexe de la baie d’Hudson (Harvey et coll. 2006). Les régions d’hivernage se trouvaient quant à elles à l’intérieur de la banquise en mouvement et dans les zones d’eaux libres du détroit d’Hudson. Dans l’ensemble, les points chauds de la période hivernale soulignent l’importance écologique des polynies et des zones de banquise pour la structure et la fonction des écosystèmes arctiques (Stirling 1997). Ainsi, la détermination des zones où les densités de prédateurs sont les plus élevées fournit des renseignements essentiels pour comprendre la dynamique du transfert énergétique dans l’Arctique et démontre ainsi l’importance de la connectivité pour les efforts de conservation.

Figure 17. Répartition spatiale de la densité du nombre d’espèces pour 21 espèces réparties sur une carte quadrillée de 50 km × 50 km illustrant les trois zones géographiques pendant la période été-automne (a, c, e) et hiver-printemps (b, d, f). La légende de la période hiver-printemps est différente de celle de la période été-automne, et les légendes varient d’une zone géographique à l’autre (source : Yurkowski et coll. 2019).
Description longue
La figure contient les graphiques de trois zones géographiques dans l’Arctique nord-américain l’été-automne (graphiques A, C et E) et l’hiver-printemps (graphiques B, D et F). Les graphiques montrent la répartition spatiale, représentée par une échelle de couleur rouge allant de pâle à foncé, pour la densité du nombre d’espèces sur 21 espèces par maille de 50 km x 50 km. La légende indiquant le nombre d’espèces par nuance de couleur pour l’hiver-printemps est différente de celle de l’été-automne, tout comme la légende entre chaque zone géographique. Les graphiques A et B illustrent la zone marine entre l’île de Baffin et le Groenland, qui s’étend vers le bas au-delà du Labrador et englobe le détroit de Lancaster dans le Nord. À l’été-automne, la plus forte densité d’individus suivis se trouve dans la portion nord de la zone, s’étendant le long de la côte est de l’île de Baffin. À l’hiver-printemps, les plus fortes densités sont observées autour de l’extrémité sud de l’île de Baffin, qui se prolonge jusqu’au Groenland. Les graphiques C et D montrent la zone marine sur le plateau de l’Alaska et de la Russie, le détroit de Béring, les mers de Tchouktches et de Beaufort et comprennent les eaux entourant les îles de Banks et de Victoria dans l’Arctique canadien. À l’été-automne, la zone est largement utilisée, et les plus fortes densités se trouvent le long de la zone du plateau des Tchouktches et de Beaufort ainsi que le long du détroit du Prince-de-Galles. En hiver-printemps, une petite partie de la zone est utilisée, et les plus fortes densités sont observées près du continent nord-américain. Les graphiques E et F couvrent la baie d’Hudson et la baie James, ainsi que le bassin Foxe et le détroit d’Hudson. La zone est largement utilisée, et les fortes densités s’étendent jusqu’à la baie d’Hudson depuis le détroit d’Hudson les deux saisons. Les fortes densités sont davantage restreintes au détroit d’Hudson pendant l’hiver-printemps que l’été‑automne.

Figure 18. Points chauds (rouge) et improductives (bleu) liées à la diversité de toutes les espèces pistées pour la période été-automne (a) et hiver-printemps (b) sur une carte quadrillée de 50 km × 50 km illustrant la zone d’étude. Les cellules de la grille ont été masquées le long du plateau continental de l’ouest du Groenland en raison du nombre moins élevé d’emplacements de marquage dans ces zones que dans les eaux canadiennes, ce qui réduit la confiance liée à la détermination des points chauds et improductives de la côte ouest du Groenland (source : Yurkowski et coll. 2019).
Description longue
Deux cartes de l’Arctique nord-américain montrant les points chauds de diversité des espèces (rouge) et les points froids (bleu foncé) par été-automne (a) et hiver-printemps (b) de toutes les espèces suivies par maille de 50 km x 50 km dans la zone d’étude. Les mailles de la carte quadrillée le long du plateau continental de l’ouest du Groenland ne sont pas incluses (c’est-à-dire qu’elles ont été masquées) en raison du nombre moins élevé d’emplacements de marquage dans ces zones que dans les eaux canadiennes, ce qui réduit la confiance dans la détermination des points chauds et des points froids de la côte ouest du Groenland. Les zones non importantes sont indiquées en jaune. L’été-automne (graphique A), il y a un point chaud dans l’ouest de l’Arctique qui s’étend du détroit de M’Clure vers l’ouest le long du plateau et du talus de Mackenzie et des Tchouktches et prend fin dans le détroit de Béring. D’autres points chauds comprennent le détroit d’Hudson, le détroit de Lancaster et des zones qui bordent le côté est de l’île de Baffin. Les points froids comprennent les zones profondes du bassin Canada ainsi que les eaux de l’Alaska et la baie James. En hiver-printemps (graphique B), le point chaud de l’ouest de l’Arctique subsiste, mais il est considérablement réduit, embrassant la zone du plateau près de la partie continentale du Canada et de l’Alaska. La zone des points chauds dans l’est de l’Arctique est beaucoup plus concentrée, centrée sur la partie sud de la baie de Baffin et bifurquant par le détroit d’Hudson et se ramifiant dans la partie nord de la baie d’Hudson. Le point chaud se ramifie vers le sud, juste au large de la côte du Labrador. Le nord de la baie de Baffin, le détroit de M’Clure et le sud de la baie d’Hudson sont des points froids. Les points chauds et les points froids sont présentés avec des intervalles de confiance à 95 %.
Encadré : Surveillance écologique par les collectivités
Lier le savoir écologique traditionnel, la science occidentale, la gestion de l’environnement et la gestion des pêches dans l’ouest de l’Arctique canadien
Burton Ayles, Comité mixte de gestion de la pêche
Les ententes sur les revendications territoriales globales conclues dans l’Arctique canadien reconnaissent le droit des Inuits d’utiliser les ressources renouvelables de la région et de participer à la gestion de ces ressources. Ils reconnaissent également les cultures traditionnelles des Inuits et la nécessité que les connaissances et les pratiques des Inuits se reflètent dans la gestion de la faune. Les gouvernements ont réagi à ces ententes et à de nombreuses affaires judiciaires en modifiant les lois, les politiques et les pratiques pour faire en sorte que le savoir autochtone et la science occidentale contribuent à appuyer la prise de décisions en matière de gestion des ressources. Toutefois, la voie à suivre pour appliquer les nombreux textes législatifs à la réalité quotidienne de la gestion et de la protection des pêches, de la faune et des habitats connexes est loin d’être claire (p. ex. Laidlaw 2015).
Au cours des dernières années, des efforts continus ont été déployés pour documenter et cataloguer les connaissances écologiques traditionnelles de l’écosystèmeNote de bas de page 1 (connaissances écologiques traditionnelles [CET]; p. ex. le Catalogue des connaissances traditionnelles et locales de la RDI, la plateforme de cartographie SIKU de la baie d’Hudson, l’inventaire des ressources côtières du Nunavut, Byers et coll. 2019). Nous décrivons ici un modèle de gestion de l’environnement et des pêches (Dorcey et Hall 1981) qui a été élargi pour inclure les CET. Il est ici appliqué à la région désignée des Inuvialuit (RDI) (Canada 1984), mais pourrait être utilisé ailleurs.
Le modèle (Figure 19) est une schématisation du lien qui existe entre la production de connaissances (CET et science occidentale) et la prise de décisions liées à l’environnement et à la gestion des pêches en vertu du cadre de cogestion établi par les revendications territoriales. L’objectif est de fournir une approche pour intégrer les CET en tant qu’outil utile de gestion des pêches et de l’environnement en reconnaissant l’importance de l’ensemble des connaissances qu’ont les Inuits à l’égard de l’environnement.
Les décisions en matière d’environnement et de gestion des pêches peuvent être perçues comme étant réparties selon un spectre ou un continuum composé de décisions à but unique, de décisions complexes à buts multiples ou de décisions intégrées. La flèche horizontale tracée au bas de la Figure 19 illustre ce continuum et fournit des exemples de processus décisionnels de la RDI qui sont régulièrement invoqués dans l’Arctique canadien. Les plans de conservation communautaires (PCC) (Comité d’étude des répercussions environnementales 2018), qui sont établis par les comités de chasseurs et de trappeurs (CCT), sont des processus clés pour la prise de décisions environnementales. Les PCC reflètent les valeurs et les objectifs de la collectivité et catégorisent l’utilisation des terres et des ressources dans la région. L’information scientifique est incluse pour compléter les CET, mais les PCC naissent dans les collectivités et sont ensuite directement liés à la planification du développement industriel proposé. Les divers processus de gestion liés au continuum décisionnel sont appuyés par des activités de recherche qui couvrent tout le spectre, allant de la description (p. ex. quelles espèces et à quel endroit) aux connaissances fonctionnelles (p. ex. les relations systémiques comme la façon dont la survie des blanchons varie en fonction de la formation de glace ou de la réponse des populations d’ombles à la pêche).
Dans le modèle, les flèches verticales noires montrent le lien qui existe entre le spectre des connaissances scientifiques et le spectre des décisions de gestion. La position relative des cinq activités de recherche et des décisions de gestion est importante. Les connaissances descriptives contribuent principalement à l’objectif et à la finalité uniques du spectre des décisions de gestion, tandis que les nouvelles connaissances fonctionnelles sont essentielles aux décisions intégrées, mais contribuent également à l’autre extrémité du spectre. Dorcey et Hall (1981) soutiennent que si l’on veut améliorer la gestion, le processus décisionnel doit être déplacé vers la droite du spectre et mettre davantage l’accent sur le soutien à l’amélioration des connaissances fonctionnelles, et donc sur la vérification d’hypothèses précises.
Les CET peuvent aussi être considérées comme s’inscrivant dans un spectre de complexité allant de simples observations individuelles à des visions et à des valeurs universelles, en passant par la gouvernance et les connaissances locales. Le long de la flèche horizontale supérieure, certaines activités relatives aux CET qui sont appuyées par la cogestion sont présentées comme un continuum de complexité. Les flèches bleues (verticale) indiquent les liens et les parallèles entre les CET et les spectres de la science, puis les liens indirects avec le spectre de gestion. Il existe également des liens directs (flèches bleues, verticale) entre le spectre des CET et le spectre de gestion. Cinq exemples sont fournis pour illustrer le flux des CET dans le modèle de gestion. La flèche bleue située à l’extrême droite indique que les récits, les croyances et les pratiques culturelles inuites peuvent influer directement sur les décisions de gestion. Dans l’ouest de l’Arctique, des aînés influents, dont Alex Aviugana et Billy Day, ont aidé à négocier la Convention définitive des Inuvialuit (Canada 1984) et ont servi avec efficacité et distinction de nombreux Inuvialuit et organismes de cogestion en apportant leurs connaissances traditionnelles aux négociations encadrées principalement par une administration publique bureaucratique occidentale (Beck 1994; Bell 2009). Plus récemment, les Inuits s’adressent directement à un public plus large sur Facebook et Twitter et dans des documentaires vidéo pour raconter leur vie et leur culture. Dans « Angry Inuk », la réalisatrice inuite Alethea Arnaquq-Baril (Arnaquq-Baril 2016) conteste l’interdiction décrétée par l’Union européenne (UE) à l’égard de l’importation du phoque. Ce faisant, elle a contribué à sensibiliser les Européens et les autres Nord-Américains au désir des Inuits d’avoir une économie durable et une source de nourriture fondées sur les ressources traditionnelles que sont le poisson et les mammifères marins plutôt que sur l’aide sociale et les produits importés du Sud. Bien que la campagne n’ait finalement pas porté ses fruits, des approches comme celle-ci peuvent tirer parti de la vision du monde que nourrissent quelque 132 000 Inuits pour aider à influencer le comportement de plus d’un milliard de personnes en Europe et en Amérique du Nord afin d’améliorer la durabilité et la protection environnementales de l’ensemble de l’Arctique.
On reproche souvent au modèle d’être fondé sur une approche bureaucratique occidentale typique de l’intégration des CET dans la gestion qui ne reflète pas adéquatement les différences réelles entre les cultures autochtones et l’idéologie dominante. Comme le soutient Stevenson (2004), cette approche peut être perçue comme une simple réappropriation des CET dans la pensée et la pratique scientifiques occidentales. C’est peut-être vrai, mais la réalité est que le système de cogestion utilisé dans l’Arctique est principalement un système étatique occidental qui exige le recours au spectre complet des CET et de la science occidentale. Le modèle proposé met en évidence les relations potentielles entre les spectres de connaissances et la façon dont ils peuvent ensemble contribuer à l’éventail des pratiques requises pour la gestion de l’environnement et des pêches dans l’Arctique. Un tel modèle devrait faciliter la communication entre les participants (p. ex. les chasseurs et pêcheurs, les scientifiques, les politiciens) et aider à concentrer les efforts des CET et de la science occidentale sur des activités précises qui sont nécessaires pour améliorer le processus décisionnel.
Le modèle présenté ici, qui est mis en œuvre dans un cadre de cogestion, promet d’améliorer l’interface entre les CET, la science occidentale et la gestion de l’environnement et des pêches. On peut affirmer, en paraphrasant White (2006), que les conseils de cogestion de l’Arctique jouent un rôle très important dans l’évaluation de l’influence des CET et qu’ils représentent la meilleure occasion d’inculquer les CET aux institutions gouvernementales publiques non autochtones. En d’autres termes, si les conseils de cogestion ne parviennent pas à intégrer les CET dans leurs processus et leurs décisions, il est peu probable qu’une autre institution publique obtienne de meilleurs résultats.

Figure 19. Modèle visuel de la relation entre les CET, les connaissances scientifiques occidentales et la prise de décisions en matière de gestion de l’environnement et des pêches.
Description longue
Un modèle visuel de la relation entre les connaissances écologiques traditionnelles (CET), les connaissances scientifiques occidentales et la prise de décisions en matière de gestion de l’environnement et des pêches. Le modèle comprend trois flèches horizontales bleues qui représentent un éventail de complexité pour 1) les connaissances traditionnelles, qui va des observations (à droite) à la vision du monde (à gauche). Voici des exemples de cet éventail : « observations sur le terrain », « surveillance de la communauté et des récoltes », « Comité de chasseurs et de trappeurs et la communauté », « ateliers et conférences sur la cogestion » et « récits, croyances, pratiques culturelles ». La deuxième flèche horizontale bleue décrit l’éventail de connaissances scientifiques, allant de descriptives (à gauche) à fonctionnelles (à droite). Parmi les exemples de cette gamme, mentionnons « inventaire, enquête », « surveillance », « analyse de bureau », « gestion adaptative » et « recherches expérimentales ». La troisième flèche horizontale bleue décrit l’éventail de la prise de décisions en matière de gestion de l’environnement et des pêches, allant des décisions ponctuelles (à gauche) aux décisions intégrées (à droite). Des exemples de cette gamme sont l’« Application des règlements de pêche [délivrance de permis et de licences] », les « Directives pour l’observation des baleines dans l’Arctique [directives, règlements] », le plan de pêche communautaire inuvialuit de la route de Tuktoyaktuk [évaluation des impacts sur les écosystèmes, plans de conservation communautaires], l’« Évaluation environnementale régionale de la mer de Beaufort [Planification globale] » et la « Protection de l’Extrême-Arctique canadien [valeurs, attitudes publiques] ».
Les flèches verticales noires montrent le lien entre l’éventail des connaissances scientifiques et l’éventail des décisions de gestion. Chaque exemple de l’éventail des connaissances scientifiques est lié à une position correspondante dans l’éventail de la prise de décisions en matière de gestion de l’environnement et des pêches.
La flèche verticale bleue montre les parallèles entre les CET et les spectres de la science, puis indirectement avec le spectre de la gestion. Il y a aussi des liens directs entre les CET et le spectre de la gestion. Cinq exemples sont fournis.
- 1) Lien entre les « observations sur le terrain » et l’« inventaire, enquête » scientifique : les Inuvialuit, les Gwich’in et les pêcheurs du Sahtu fournissent des données primaires pour évaluer les migrations du saumon.
- 2 et 3) lien entre le « CCT et la communauté » et la prise de décisions fondée sur les études d’impact sur l’environnement (EIE) et les programmes canadiens de certification (PCC).
- Le plan de gestion de la pêche de subsistance et récréative durable le long de la route de Tuktoyaktuk est fondé principalement sur les CET de la communauté.
- Dans les années 1990 et 2000, la planification de l’exploration et de la mise en valeur du pétrole et du gaz a été guidée par les plans d’aménagement du territoire énoncés dans les PCC.
- 4) Lien entre les « ateliers et conférences sur la cogestion » et la « gestion adaptative » scientifique : le Sommet sur le béluga de 2016, organisé par le MPO, le Comité mixte de gestion de la pêche (CMGP) et le Conseil Inuvialuit de gestion du gibier, a produit un état des connaissances sur le béluga qui a accordé la même importance aux CET et à la science occidentale.
- 5) Lien entre « récits, croyances, pratiques culturelles » et « décision intégrée » de la gestion : la représentation des aînés (p. ex. négociations de la Convention définitive des Inuvialuit) et les récentes activités multimédias ont permis de faire connaître la vie et la culture inuites au grand public.
Science participative à la mode de l’Arctique
Karen Dunmall et Kim Howland, Pêches et Océans Canada

Figure 20. Brandon Green et Steve Illasiak en train de traiter des échantillons de poissons et d’enregistrer des données biologiques dans la zone de protection marine d’Anguniaqvia niqiqyuam, Territoires du Nord-Ouest, 2018 (photo : Darcy McNicholl).
L’évolution rapide de l’Arctique comporte des défis tant pour les scientifiques qui évaluent les répercussions et les possibilités que pour les peuples autochtones qui entretiennent de très étroites relations avec l’environnement et ses ressources. La biodiversité de l’Arctique est irrévocablement liée à la culture des peuples autochtones du Nord, et leur perception du changement est enracinée dans leur dépendance à l’égard de l’environnement et dans leur incarnation des valeurs sociales axées sur la protection des moyens de subsistance (CAFF 2013). En fait, le manque d’information scientifique sur les espèces et leurs habitats dans l’Arctique (Reist et coll. 2006a) contraste avec l’étendue des connaissances des Inuits sur l’environnement. Par conséquent, le fait d’offrir la possibilité novatrice d’évaluer le changement à ceux qui observent directement les effets immédiats sur l’environnement constitue une approche puissante pour renforcer l’influence humaine sur le rythme de la science et le rythme du changement. Dans l’Arctique canadien, la science participative peut être un important outil de surveillance écologique par les collectivités permettant de faire le pont entre le savoir autochtone et la recherche scientifique en vue d’aboutir ultimement à la coproduction du savoir (Dunmall et Reist 2018).
L’utilisation commune d’indicateurs précis et faciles à documenter pour évaluer les changements environnementaux dans les systèmes de connaissances autochtones et scientifiques constitue le fondement de la science participative dans l’Arctique canadien (Dunmall et Reist 2018). Les connaissances contemporaines acquises grâce à la surveillance de l’environnement au moyen d’indicateurs peuvent se traduire par l’établissement de données de référence et la surveillance quantitative des changements écologiques, à petite comme à grande échelle spatiale. Bien que la vaste série d’indicateurs habituellement recueillis par le savoir autochtone soit souvent différente des indicateurs précis qui sont utilisés dans la recherche scientifique, ces deux méthodes de surveillance sont liées et peuvent mettre en évidence des changements similaires au niveau des écosystèmes (Riedlinger et Berkes 2001; Berkes et coll. 2007; Tremblay et coll. 2008). La communication et la sensibilisation sont essentielles au succès de la science participative dans l’Arctique et sont facilitées en partie par l’utilisation des médias sociaux (p. ex. Facebook) pour diffuser l’information et interagir avec les participants et les observateurs (Dunmall et Reist 2018).
La prévalence de la surveillance écologique par les collectivités augmente dans l’Arctique canadien. Le programme sur le saumon arctique (www.facebook.com/arcticsalmon) utilise une approche axée sur la surveillance par les collectivités pour faire la pistage de l’augmentation de l’abondance et de l’élargissement de la répartition du saumon du Pacifique (espèces Oncorhynchus) et des changements liés à la répartition des poissons dans l’Arctique canadien (Dunmall et coll. 2013, 2017, 2018). La surveillance écologique des bélugas (Delphinapterus leucas) basée sur la chasse fournit des données importantes sur la santé et l’état corporel des bélugas grâce au prélèvement d’échantillons et à la mesure d’indicateurs particuliers (Loseto et coll. 2018c). La surveillance de l’environnement physique par les collectivités, y compris l’acquisition de connaissances inuites, se fait également dans la baie d’Hudson (p. ex. Arctic Eider Society https://arcticeider.com/siku). La surveillance de l’écosystème côtier par les collectivités, y compris la collecte de données sur les paramètres environnementaux, la production primaire, les habitats benthiques et la biodiversité des poissons, se poursuit dans la baie Darnley (Territoires du Nord‑Ouest) depuis 2012 (McNicholl et coll. 2017) et a récemment été transformée en un cadre de surveillance écologique par les collectivités dont la transférabilité aux environnements côtiers situés près de Kugluktuk (Nunavut) de Sachs Harbour (Territoires du Nord-Ouest) a été mise à l’essai en 2017 et 2018, respectivement (McNicholl et Dunmall 2018a). Dans les collectivités où l’activité maritime est relativement élevée et où le risque d’espèces envahissantes est donc plus important, des techniques d’enquête portuaire communautaire et d’échantillonnage de l’ADN environnemental (ADNe) ont été introduites (2015-2018 : Churchill [Manitoba], Salluit [Nunavik], Iqaluit et Pond Inlet [Nunavut] (Polar Knowledge Canada 2017). Ces efforts ont été combinés à des ateliers éducatifs axés sur les jeunes pour les sensibiliser et leur fournir des guides d’identification et une formation pratique sur la façon de signaler de nouvelles observations et de distinguer les espèces envahissantes qui présentent un risque élevé des espèces indigènes similaires.

Figure 21. Modèle établi pour la science participative afin de surveiller l’évolution de l’Arctique canadien. Dans le cadre d’une priorité commune de surveillance des changements environnementaux, la science participative (carré gris) peut faire le pont entre les systèmes de connaissances autochtones et scientifiques (cercles blancs). Les flèches représentent le flux contributif d’information provenant du cadre général de la science participative (rectangle noir) qui est dirigé vers chaque système de connaissances et de nouveau vers le cadre à chaque étape du processus, ce qui égalise la valeur de l’information tirée des connaissances scientifiques et des connaissances autochtones et contribue à la coproduction du savoir. Un élément clé du modèle est le processus interactif d’établissement de rapports et les communications continues entre les participants (source : Dunmall et Reist 2018).
Description longue
Un modèle descriptif (travail et flèches) de la science citoyenne ayant pour but de surveiller l’évolution de l’Arctique canadien. Dans le cadre d’une priorité commune de surveillance des changements environnementaux, la science citoyenne (carré gris) peut faire le pont entre les systèmes de connaissances autochtones et scientifiques (indiqué par des cercles blancs). La science citoyenne dans le cadre d’un système de connaissances autochtones peut se décrire comme suit ou comprendre les éléments suivants : vaste série, observation, accent mis sur l’oral, accent contemporain et historique, valeur traditionnelle et culturelle. Par comparaison, la science citoyenne dans le cadre d’un système de connaissances scientifiques peut se décrire comme suit ou comprendre les éléments suivants : mesure précise/unique, accent écrit, accent contemporain et futur, hypothèses et objectifs.
Les flèches représentent le flux contributif d’information du cadre général de la science citoyenne (case noire avec les étapes : définir l’indicateur, consigner, rapporter, analyser, évaluer) vers chaque système de connaissances et vers le cadre à chaque étape du processus, ce qui égalise la valeur de l’information dérivée des connaissances scientifiques et des connaissances autochtones et contribue à la coproduction du savoir. Un élément clé est le processus interactif d’établissement de rapports et les communications continues entre les participants.
La surveillance par les collectivités est en train d’émerger dans l’Arctique canadien. Il s’agit là d’un changement subtil, mais très important, lié au rôle de leadership qu’exercent les peuples autochtones dans tous les aspects des efforts de surveillance déployés sur le terrain en vertu d’un cadre de collaboration fondé sur la science. La transition vers cet effort entrepris par les collectivités est un processus qui exige du temps et une communication efficace, de la motivation et l’établissement d’un commun accord en ce qui a trait aux indicateurs et aux objectifs, ainsi que le renforcement des capacités grâce à la mise en place de protocoles, d’équipement et de formation. Les efforts de surveillance menés par la collectivité dans la zone de protection marine d’Anguniaqvia niqiqyuam, près de Paulatuk (Territoires du Nord-Ouest), ont permis en 2018 de recueillir des données sur des indicateurs couvrant plusieurs niveaux trophiques, ainsi que des données environnementales concernant l’écosystème côtier (McNicholl et Dunmall 2018b) (Figure 20). Le leadership en matière de surveillance écologique des bélugas a été constant chez les Inuvialuit, et la récente acquisition de CET (Ostertag et coll. 2018; Waugh et coll. 2018) complète ces efforts en fournissant un contexte écosystémique à des indicateurs précis (Loseto et coll. 2018c).
La science participative est un outil très attrayant pour évaluer les changements environnementaux dans l’Arctique. Lorsqu’elle est appliquée avec soin dans le cadre d’un modèle qui met l’accent sur la communication continue et efficace et qui assure la production concertée de connaissances (Figure 21), la science participative peut fournir l’information essentielle nécessaire pour prévoir les répercussions et les possibilités associées aux changements de la biodiversité et à l’évolution rapide des écosystèmes dans l’Arctique. De plus, si elle est appliquée de façon cohérente à l’aide d’un cadre commun, la science participative pratiquée par les peuples autochtones offre une vaste couverture géographique et une surveillance écologique à long terme, ce qui permet de mieux comprendre la nature, les tendances et les conséquences des changements qui ont cours dans l’Arctique. Il en résultera une cogestion des ressources et une gérance environnementale plus efficaces.
Encadré : Intégration des connaissances
Surveillance écologique et gestion du béluga, et relations humaines
Lisa Loseto, Elizabeth Worden, Pêches et Océans Canada

Figure 22. Processus suivi pour sélectionner les indicateurs de santé des bélugas avec les localités d’Inuvik, de Tuktoyaktuk et de Paulatuk (source : Ostertag et coll. 2019).
Description longue
L’image illustre le processus suivi afin de sélectionner les indicateurs de santé des bélugas avec les communautés d’Inuvik, de Tuktoyaktuk et de Paulatuk. Chaque étape (flèche recourbée) contribue à la suivante. Les étapes sont les rencontres publiques, les questionnaires et les entrevues, les groupes de discussion, l’examen et la sélection des indicateurs.
Chaque été, des milliers de bélugas de l’est de la mer de Beaufort, les qilalukkaqs (Delphinapterus leucas), se regroupent dans l’estuaire du Mackenzie, dans les eaux canadiennes de la mer de Beaufort. Cette population est reconnue comme étant l’une des plus importantes au Canada, avec environ 40 000 individus (Harwood 1996; Hill et Demaster 1999). La chasse de subsistance de ces bélugas par les Inuvialuit, les Inuits de l’ouest de l’Arctique canadien, a eu et continue d’avoir une grande importance économique, alimentaire et culturelle. Les bélugas de l’est de la mer de Beaufort sont cogérés par Pêches et Océans Canada (MPO) et le Comité mixte de gestion de la pêche (CMGP) sous la direction du Conseil inuvialuit de gestion du gibier, conformément à la Convention définitive des Inuvialuit (Canada 1984). La Convention définitive des Inuvialuit, le Plan de gestion du béluga de la mer de Beaufort et les efforts antérieurs de gestion de la conservation ont appuyé la collecte de données sur les prises de bélugas grâce à l’établissement de partenariats entre les organismes de cogestion et à la collaboration avec les comités locaux de chasseurs et de trappeurs (CCT).
Par conséquent, des données sur le béluga de l’est de la mer de Beaufort ont été recueillies pendant plus de 40 ans dans le cadre du programme de surveillance écologique des prises, un programme de surveillance écologique par les collectivités (Harwood et coll. 2002). Le programme a évolué pour devenir un point central réunissant des scientifiques, des membres de la collectivité et des conseils de cogestion qui travaillent en équipe pour répondre aux préoccupations de la collectivité et définir l’orientation de la recherche. En 2010, les zones de gestion du béluga désignées 1a sont devenues la première zone de protection marine de l’Arctique, la zone de protection marine (ZPM) de Tarium Niruitait (Loseto et coll. 2010). Une partie du cadre de surveillance et de gestion de la ZPM comprend le recours à des indicateurs qui sont utilisés pour mesurer et communiquer la santé de la ZPM. Au cours des 10 dernières années, le programme de surveillance écologique par les collectivités existant a pris de l’ampleur et de la profondeur pour inclure des indicateurs sur l’état du béluga, son régime alimentaire et sa santé, ce qui comprend la surveillance écologique des contaminants et des maladies et d’autres indicateurs physiologiques qui peuvent également être extrapolés à la santé des écosystèmes (Loseto et coll. 2018b). Même si la surveillance s’est élargie pour inclure de multiples indicateurs de santé et indicateurs écologiques, on a noté que le programme de surveillance écologique par les collectivités ne disposait d’aucun mécanisme pour inclure les vastes connaissances inuites, appelées connaissances écologiques locales et traditionnelles (CEL, CET), détenues par les Inuvialuit dans la RDI.
Les Inuvialuit et leurs ancêtres gèrent la population de façon durable depuis des centaines d’années (McGhee 1988; FJMC 2013). Ils ont acquis une connaissance approfondie du comportement et des caractéristiques liées à la santé des bélugas de la RDI. Grâce à l’établissement de relations de travail à long terme lors des activités de collaboration menées dans le cadre de divers projets liés au béluga, un projet a été lancé pour combler les lacunes relatives à l’intégration des CEL et des CET au programme de surveillance écologique par les collectivités axé sur le béluga (S. Ostertag, données non publiées). Dans le cadre d’un vaste processus de consultation (2012-2017), des indicateurs de l’état de santé et de la présence de maladies chez les bélugas ont été établis par les détenteurs de connaissances sur les bélugas dans les trois collectivités les plus actives dans la RDI : les localités d’Inuvik, de Tuktoyaktuk et de Paulatuk (S. Ostertag, données non publiées). Ce processus a mis l’accent sur le partage des connaissances des Inuvialuit, la communication fréquente et la rétroaction collaborative à diverses étapes de la recherche (S. Ostertag, données non publiées ) (Figure 22). Voici des exemples d’indicateurs établis par les trois collectivités : la couleur et la texture de la graisse ou uqsuq, la forme du corps (dos large ou rond, rouleaux de graisse décrits comme des « poignées d’amour ») et les signes d’infection. Ces indicateurs ont maintenant été intégrés au programme de surveillance écologique par les communautés des poissons et des mammifères marins du CMGP afin de garantir que les observations des Inuits sur la santé et l’état corporel des bélugas sont consignées pour les bélugas prélevés (Figure 23).

Figure 23. Fiche de surveillance des bélugas du CMGP/MPO (feuille 1 de 2) qui comprend des indicateurs basés sur les CET.
Description longue
Une photographie de la fiche de suivi des bélugas du CMGP/MPO (feuille 1 de 2) qui comprend des indicateurs basés sur les CET. L’information recueillie comprend la couleur (choix proposés), la présence de poignées d’amour (oui/non) et la forme de la colonne vertébrale. Les signes d’infection, blessures ou anomalies sont consignés. La fiche comporte également une section dans laquelle on peut dessiner les anomalies sur des diagrammes de baleines (vue du haut, de droite ou de gauche de la baleine). Une section permet également d’indiquer quel dessin ressemble au dos de la baleine vu de devant et de derrière.
Le succès des indicateurs de santé des bélugas établis par les collectivités est en grande partie attribuable aux observations annuelles répétées des pêcheurs actifs sur le terrain et à leurs interactions avec les bélugas. Les connaissances des Inuvialuit sur la chasse au béluga sont dynamiques et bien ancrées dans la tradition transmise par l’histoire orale, mais aussi dans les observations locales en constante évolution. Cependant, malgré ces activités intergénérationnelles de chasse au béluga, des changements récents – tant environnementaux que sociaux – ont eu des répercussions sur les relations entre l’homme et le béluga dans la région. Par exemple, la communauté d’Aklavik, qui a une longue tradition de chasse au béluga active, a connu un déclin marqué de ses prises annuelles de baleines (Worden 2018) (Figure 24).

Figure 24. Récolte annuelle des bélugas d’Aklavik de 1975 à 2013 (source : CMGP).
Description longue
Graphique linéaire de la récolte annuelle des bélugas d’Aklavik (nombre de baleine de 0 à 38) (axe des ordonnées latéral) de 1975 à 2013 (axe des abscisses en bas). Une ligne de tendance pour toutes les données indique une tendance à la baisse importante (valeur R2 de 0,6707). Entre 1976 et 1999, le nombre de prises a varié entre 12 et 35. Depuis 2000, le nombre de prises est inférieur à 10 par année.
Références Citées
Ardyna, M., Babin, M., Gosselin, M., Devred, E., Rainville, L., et Tremblay, J.-É. 2014. Recent Arctic Ocean sea ice loss triggers novel fall phytoplankton blooms. Geophys. Res. Lett. 41: 6207–6212. doi: 10.1002/2014GL061047.
Arnaquq-Baril, A. 2016. Angry Inuk https://www.nfb.ca/film/angry_inuk/ [Video].
Arrigo, K.R., Perovich, D.K., Pickart, R.S., Brown, Z.W., van Dijken, G.L., Lowry, K.E., Mills, M.M., Palmer, M.A., Balch, W.M., Bahr, F., Bates, N.R., Benitez-Nelson, C., Bowler, B., Brownlee, E., Ehn, J.K., Frey, K.E., Garley, R., Laney, S.R., Lubelczyk, L., Mathis, J., Matsuoka, A., Mitchell, B.G., Moore, G.W.K., Ortega-Retuerta, E., Pal, S., Polashenski, C.M., Reynolds, R.A., Scheiber, B., Sosik, H.M., Stephens, M., et Swift, J.H. 2012. Massive phytoplankton blooms under Arctic sea ice. Science 336: 1408. doi: 10.1126/science.1215065.
Barber, D.G., Hop, H., Mundy, C.J., Else, B., Dmitrenko, I.A., Tremblay, J.-É., Ehn, J.K., Assmy, P., Daase, M., Candlish,L.M., et Rysgaard, S. 2015. Selected physical, biological et biogeochemical implications of a rapidly changing arctic marginal ice zone. Prog. Oceanogr. 139: 122–150. doi: 10.1016/j.pocean.2015.09.003.
Beck, T. 1994. Alexander Charles Aviugana (1945–1994). Arctic 47: 319. doi: 10.14430/arctic1302.
Bell, R. 2009. Billy Joseph Day, whale hunter, trapper, environmentalist, September 15, 1930–July 16, 2008. Globe et Mail, Lives Lived. 2009, 21 January.
Berkes, F., Colding, J., et Folke, C. 2000. Rediscovery of traditional ecological knowledge as adaptive management. Ecol. Appl. 10: 1251–1262. doi: 10.2307/2641280.
Berkes, F., Berkes, M.K., et Fast, H. 2007. Collaborative integrated management in Canada's North: The role of local et traditional knowledge et community-based monitoring. Coast. Manage. 35: 143–162. doi: 10.1080/08920750600970487.
Blais, M., Ardyna, M., Gosselin, M., Dumont, D., Bélanger, S., Tremblay, J.-É., Gratton, Y., Marchese, C., et Poulin, M. 2017. Contrasting interannual changes in phytoplankton productivity et community structure in the coastal Canadian Arctic Ocean. Limnol. Oceanogr. 62 : 2480–2497. doi: 10.1002/lno.10581.
Bouchard, C., Geoffroy, M., LeBlanc, M., Majewski, A., Gauthier, S., Walkusz, W., Reist, J.D., et Fortier, L. 2017. Climate warming enhances polar cod recruitment, at least transiently, Prog. Oceanogr. 156: 121–129. doi: 10.1016/j.pocean.2017.06.008
Boyce, D.G., Frank, K.T., Worm, B., et Leggett, W.C. 2015. Spatial patterns et predictors of trophic control in marine ecosystems. Ecol. Lett. 18: 1001–1011. doi: 10.1111/ele.12481
Breed, G.A., Matthews, C.J.D., Marcoux, M., Higdon, J.W., LeBlanc, B., Petersen, S.D., Orr, J., Reinhart, N.R., et Ferguson, S.H. 2017. Sustained disruption of narwhal habitat use et behaviour in the presence of Arctic killer whales. Proc. Natl. Acad. Sci. USA 114: 2628–2633. doi: 10.1073/pnas.1611707114.
Burnham, K.K., Johnson, J.A., Konkel, B., et Burnham, J.L. 2012. Nesting common eider (Somateria mollissima) population quintuples in Northwest Greenland. Arctic 65: 456–464. doi: 10.14430/arctic4243.
Byers, T., Reist, J.D., et Sawatzky, C.D. 2019. Compilation et synopsis of literature on the traditional knowledge of Indigenous peoples in the Northwest Territories concerning Dolly Varden. Can. Manuscr. Rep. Fish. Aquat. Sci. 3177: vi + 63 p. Available from http://publications.gc.ca/site/eng/9.873211/publication.html [accessed 3 October 2019].
CAFF. 2013. Arctic biodiversity assessment: Status et trends in Arctic biodiversity. Conservation of Arctic Flora et Fauna, Akureyri, Iceland. 674 p. Available from https://oaarchive.arctic-council.org/handle/11374/223 [accessed 20 February 2019].
Canada. 1984. The Western Arctic claim: The Inuvialuit Final Agreement. Indian et Northern Affairs Canada, Ottawa. 259p. Available from http://webarchive.bac-lac.gc.ca:8080/wayback/20060205004956/http://www.ainc-inac.gc.ca/pr/agr/inu/wesar_e.pdf [accessed 08 February 2019].
Carmack, E.C., et Chapman, D.C. 2003. Wind‐driven shelf/basin exchange on an Arctic shelf: The joint roles of ice cover extent et shelf‐break bathymetry. Geophys. Res. Lett. 30: 1778. doi: 10.1029/2003GL017526.
Chambault, P., Albertsen, C.M., Patterson, T.A., Hanse, R.G., Tervo, O., Laidre, K.L., et Heide-Jørgensen, M.P. 2018. Sea surface temperature predicts the movements of an Arctic cetacean: The bowhead whale. Sci. Rep. 8: 9658. doi: 10.1038/s41598-018-27966-1.
Choy, E.S., Rosenberg, B., Roth, J.D., et Loseto, L.L. 2017. Inter-annual variation in environmental factors affect the prey et body condition of beluga whales in the eastern Beaufort Sea. Mar. Ecol. Prog. Ser. 579: 213–225. doi: 10.3354/meps12256.
Coupel, P., Matsuoka, A., Diana, R.P., Gosselin, M., Marie, D., Tremblay, J.-É., et Babin, M. 2015. Pigment signatures of phytoplankton communities in the Beaufort Sea. Biogeosciences 12: 991–1006. doi: 10.5194/bg-12-991-2015.
Davidson, T.A., Wetterich, S., Johansen, K.L., Grønnow, B., Windirsch, T., Jeppesen, E., Syvaranta, J., Olsen, J., González-Bergonzoni, I., Strunk, A., Larsen, N.K., Meyer, H., Søndergaard, J., Dietz, R., Eulears, I., et Mosbech, A. 2018. The history of seabird colonies et the North Water ecosystem: Contributions from palaeoecological et archaeological evidence. Ambio 47: 175–192. doi: 10.1007/s13280-018-1031-1.
Deming, J.W., Fortier, L., et Fukuchi, M. 2002. The International North Water Polynya Study (NOW): A brief overview. Deep-Sea Res. II 49: 4887–4892. doi: 10.1016/S0967-0645(02)00168-6.
DFO. 2015. Anguniaqvia Niqiqyuam area of interest: Monitoring indicators, protocols et strategies (PDF, 485 KB). DFO Can. Sci. Advis. Sec. Sci. Advis. Rep. 2015/025. Available from https://waves-vagues.dfo-mpo.gc.ca/library-bibliotheque/364882.pdf [accessed 08 February 2019].
Dorcey, A.H.J., et Hall, K.J. 1981. Setting ecological research priorities for management: The art of the impossible in the Fraser estuary. Westwater Research Centre, The University of British Columbia. Vancouver, B.C. 78p.
Dunmall, K.M., et Reist J.D. 2018. Developing a citizen science framework for the Arctic using the ‘Arctic Salmon’ initiative. In Impacts of a Changing Environment on the Dynamics of High-latitude Fish et Fisheries. Edited by F.J. Mueter, M.R. Baker, S.C. Dressel, et A.B. Hollowed. Alaska Sea Grant, University of Alaska Fairbanks. pp. 31–47. doi: 10.4027/icedhlff.2018.02.
Dunmall, K.M., Reist, J.D., Carmack, E.C., Babaluk, J.A., Heide-Jørgensen, M.P., et Docker, M.F. 2013. Pacific salmon in the Arctic: Harbingers of change. In Responses of Arctic Marine Ecosystems to Climate Change. Edited by F.J. Mueter, D.M.S. Dickson, H.P. Huntington, J.R. Irvine, E.A. Logerwell, S.A. MacLean, L.T. Quakenbush, et C. Rosa. Alaska Sea Grant, University of Alaska Fairbanks. pp. 141–163. doi: 10.4027/ramecc.2013.07.
Dunmall, K.M., Gruben, M., McNicholl, D., et Reist, J. 2017. Arctic Salmon: Linking subsistence et science to track et predict changing biodiversity of fishes in the Canadian Arctic. Integrated Regional Impact Study of the western et central Canadian Arctic (IRIS 1), December 2017 newsletter. ArcticNet. Available from http://www.arcticnet.ulaval.ca/media/iris_reports.php [accessed 08 February 2019].
Dunmall, K.M., McNicholl, D.G., et Reist, J.D. 2018. Community-based monitoring demonstrates increasing occurrences et abundances of Pacific salmon in the Canadian Arctic from 2000 to 2017. North Pacific Anadromous Fish Commission Technical Report 11: 87–90. [accessed 08 February 2019].
Dyck, M., Campbell, M., Lee, D.S., Boulanger, J., et Hedman, D. 2017. 2016 Aerial survey of the western Hudson Bay polar bear sub-population (PDF, 3.67 MB). Final Report. Government of Nunavut, Department of Environment, Wildlife Research Section, Status Report 2017-xx, Igloolik, NU. 82 pp + 2 Supplements.
Egevang, C., Boertmann, D., Mosbech, A., et Tamstorf, M.P. 2003. Estimating colony area et population size of little auks Alle alle at Northumberland Island using aerial images. Polar Biol. 26: 8–13. doi: 10.1007/s00300-002-0448-x.
EISC. 2018. Inuvialuit Environmental Impact Screening Committee. Community Conservation Plans. Available from http://www.screeningcommittee.ca/resources/inuvialuit.html [accessed 13 September 2018].
Ferguson, S.H., Kingsley, M.C.S., et Higdon, J.W. 2012. Killer whale (Orcinus orca) predation in a multi-prey system. Popul. Ecol. 54: 31–41. doi: 10.1007/s10144-011-0284-3.
Ferguson, S.H., Young, B.G., Yurkowski, D.J., Anderson, R., Willing, C., et Nielsen, O. 2017. Demographic, ecological, et physiological responses of ringed seals to an abrupt decline in sea ice availability. PeerJ 5: e2957. doi: 10.7717/peerj.2957. PMID:28168119.
FJMC [Fisheries Joint Management Committee]. 2013. Beaufort Sea beluga management plan. 4th amended printing (PDF, 866 KB). Available from https://www.beaufortseapartnership.ca/wp-content/uploads/2015/04/Beaufort-Sea-Beluga-Management-Plan-2013.pdf [accessed 15 September 2018].
FJMC [Fisheries Joint Management Committee]. 2017. One people one plan: Inuvialuit plan for fishing on the Inuvik to Tuktoyaktuk highway (PDF, 127 KB). 5 p. Available from https://fjmc.ca/wp-content/uploads/2017/11/ITH-Community-Fishing-Plan-2017-02.pdf [accessed 15 September 2018].
Grebmeier, J.M., Cooper, L.W., Feder, H.M., et Sirenko, B.I. 2006. Ecosystem dynamics of the Pacific-influenced Northern Bering et Chukchi Seas in the Amerasian Arctic. Prog. Oceanogr. 71: 331–361. doi: 10.1016/j.pocean.2006.10.001.
Harvey, M., Starr, M., Therriault, J.C., Saucier, F., et Gosselin, M. 2006. MERICA-Nord Program: Monitoring et research in the Hudson Bay complex (PDF, 3.69 MB). AZMP Bulletin 5: 27–32. Available at https://waves-vagues.dfo-mpo.gc.ca/library-bibliotheque/365692.pdf [accessed 08 February 2019].
Harwood, L.A., Innes, S., Norton, P., et Kingsley, M.C.S. 1996. Distribution et abundance of beluga whales in the Mackenzie estuary, southeast Beaufort Sea, et west Amundsen Gulf during late July 1992. Can. J. Fish. Aquat. Sci. 53: 2262–2273. doi: 10.1139/f96-180.
Harwood, L.A., Norton, P., Day, B., et Hall, P.A. 2002. The harvest of beluga whales in Canada's western Arctic: Hunter-based monitoring of the size et composition of the catch. Arctic 55: 10–20. doi: 10.14430/arctic687.
Harwood, L.A., Smith, T.G., Georges, C., Sandstrom, S., Walkusz, W., et Divoky, G.J. 2015a. Change in the Beaufort Sea ecosystem: Diverging trends in body condition and/or production in five marine vertebrate species. Progr. Oceanogr. 136: 263–273.
doi: 10.1016/j.pocean.2015.05.003.
Harwood, L., Kingsley, M.C.S., et Pokiak, F. 2015b. Monitoring beluga harvests in the Mackenzie Delta et near Paulatuk, NT, Canada: Harvest efficiency et trend, size et sex of landed whales, et reproduction, 1970–2009. Can. Manuscr. Rep. Fish. Aquat. Sci.. 3059: vi + 32 p. Available from http://publications.gc.ca/collections/collection_2015/mpo-dfo/Fs97-4-3059-eng.pdf [accessed 08 February 2019].
Hauser, D.D.W., Laidre, K.L., Stern, H.L., Moore, S.E., Suydam, R.S., et Richard, P.R. 2017. Habitat selection by two beluga whale populations in the Chukchi et Beaufort seas. PLoS ONE 12: e0172755. doi: 10.1371/journal.pone.0172755.
Heide-Jørgensen, M.P., Strander Sinding, M.-H., Nielsen, N.H., Rosing-Asvid, A., et Hansen, R.G. 2013. The significance of the North Water polynya to arctic top predators. Ambio 42: 596–610. doi: 10.1007/s13280-012-0357-3.
Heide-Jørgensen, M.P., Sinding, M.H.S., Nielsen, N.H., Rosing-Asvid, A., et Hansen, R. G. 2016. Large numbers of marine mammals winter in the North Water polynya. Polar Biol. 39: 1605–1614. doi: 10.1007/s00300-015-1885-7.
Higdon, J.W., et Ferguson, S.H. 2009. Loss of Arctic sea ice causing punctuated change in sightings of killer whales (Orcinus orca) over the past century. Ecol. Appl. 19: 1365–1375. doi: 10.1890/07-1941.1.
Higdon, J.W., et Ferguson, S.H. 2014. Inuit recollections of a 1950s killer whale (Orcinus orca) ice entrapment in Foxe Basin, Nunavut, Canada. Aquat. Mamm 40: 9–19. doi: 10.1578/AM.40.1.2014.9.
Higdon, J.W., Westdal, K.H., et Ferguson, S.H. 2013. Distribution et abundance of killer whales (Orcinus orca) in Nunavut, Canada – an Inuit knowledge survey. J. Mar. Biol. Assoc. U.K. 94: 1293–1304. doi: 10.1017/S0025315413000921.
Hill, P.S., et DeMaster, D.P. 1999. Alaska marine mammal stock assessments, 1999. NOAA Techinical Memorandum NMFS-AFSC-110: iii + 174 p. Available from ftp://ftp.library.noaa.gov/noaa_documents.lib/NMFS/AFSC/TM_AFSC/TM_NMFS_AFSC_110.pdf [accessed 08 February 2019].
Hornby, C.A., Hoover, C., Iacozza, J., Barber, D.G., et Loseto, L.L. 2016. Spring conditions et habitat use of beluga whales (Delphinapterus leucas) during arrival to the Mackenzie River Estuary. Polar Biol. 39: 2319–2334. doi: 10.1007/s00300-016-1899-9.
Hornby, C.A., Iacozza, J., Hoover, C., Barber, D.G., et Loseto, L.L. 2017. Beluga whale Delphinapterus leucas late summer habitat use et support for foraging areas in the Canadian Beaufort Sea. Mar. Ecol. Prog. Ser. 574: 243–257. doi: 10.3354/meps12178.
Horvat, C., Jones, D.R., Iams, S., Schroeder, D., Flocco, D., and Feltham, D. 2017. The frequency and extent of sub-ice phytoplankton blooms in the Arctic Ocean. Sci. Adv. 3: e1601191. doi:10.1126/sciadv.1601191.
Hussey, N.E., Kessel, S.T., Aarestrup, K., Cooke, S.J., Cowley, P.D., Fisk, A.T., Harcourt, R.G., Holland, K.N., Iverson, S.J., Kocik, J.F., Mills Flemming, J.E., and Whoriskey, F.G. 2015. Aquatic animal telemetry: A panaromic window into the underwater world. Science 348: 1221. doi: 10.1126/science.1255642.
IPCC. 2014. Climate change 2014: Synthesis report. Contribution of Working Groups I, II and III to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change [Core Writing Team, R.K. Pachauri and L.A. Meyer (eds.)]. IPCC, Geneva, Switzerland. 151 p. Available from https://www.ipcc.ch/report/ar5/syr/ [accessed 08 February 2019].
Irvine, J.R., and Riddell, B.E. 2007. Salmon as status indicators for North Pacific ecosystems (anglais seulement). N. Pac. Anadr. Fish Comm. Bull. 4: 285–287. Available from https://npafc.org/wp-content/uploads/2017/09/bulletin4.pdf [accessed 08 February 2019].
Jeppesen, E., Appelt, M., Hastrup, K., Grønnow, B., Mosbech, A., Smol, J.P., and Davidson, T.A. 2018. Living in an oasis: Rapid transformations, resilience, and resistance in the North Water Area societies and ecosystems. Ambio 47: 296–309. doi: 10.1007/s13280-018-1034-y.
Kovacs, K., and Michel, C. 2011. Biological impacts of changes to sea ice in the Arctic. In Snow, Water, Ice and Permafrost in the Arctic (SWIPA): Climate Change and the Cryosphere. Arctic Monitoring and Assessment Programme (AMAP), Oslo, Norway. pp. 9-32–9-51. Available from https://www.amap.no/documents/doc/snow-water-ice-and-permafrost-in-the-arctic-swipa-climate-change-and-the-cryosphere/743 [accessed 08 February 2019].
Laidlaw, D. 2015. Challenges in using Aboriginal traditional knowledge in the courts. In A Symposium on Environment in the Courtroom: Evidentiary Issues in Environmental Prosecutions and Hearings, March 6-7, 2015. University of Calgary.
Lewis, A.E., Hammill, M.O., Power, M., Doidge, D.W., and Lesage, V. 2009. Movement and aggregation of eastern Hudson Bay beluga whales (Delphinapterus leucas): A comparison of patterns found through satellite telemetry and Nunavik traditional ecological knowledge. Arctic 62: 13–24. doi: 10.14430/arctic109.
Loseto, L.L., Stern, G.A., Connelly, T.L., Deibel, D., Gemmill, B., Prokopowicz, A., Fortier, L., and Ferguson, S.H. 2009. Summer diet of beluga whales inferred by fatty acid analysis of the eastern Beaufort Sea food web. J. Exp. Mar. Biol. Ecol. 374: 12–18. doi: 10.1016/j.jembe.2009.03.015.
Loseto, L., Wazny, T., Cleator, H., Ayles, B., Cobb, D., Harwood, L., Michel, C., Nielsen, O., Paulic, J., Postma, L., Ramlal, P., Richard, P., Ross, P.S., Solomon, S., Walkusz, W., Weilgart, L., and Williams, B. 2010. Information in Support of Indicator Selection for Monitoring the Tarium Niryutait Marine Protected Area (TN MPA). DFO Can. Sci. Advis. Sec. Res. Doc. 2010/094. iv + 42 p. Available from www.dfo-mpo.gc.ca/csas-sccs/Publications/ResDocs-DocRech/2010/2010_094-eng.html [accessed 08 February 2019].
Loseto, L.L., Brewster, J.D., Ostertag, S.K., Snow, K., MacPhee, S.A., McNicholl, D.G., Choy, E.S., Giraldo, C., and Hornby, C.A. 2018a. Diet and feeding observations from an unusual beluga harvest in 2014 near Ulukhaktok, Northwest Territories, Canada. Arctic Science 4: 421–431. doi: 10.1139/as-2017-0046.
Loseto, L.L., Lam, J., and Iacozza, J. (eds.). 2018b. Beluga Summit: knowledge sharing of the eastern Beaufort Sea beluga whale. Arctic Science 4: i–iv. doi: 10.1139/as-2018-0011.
Loseto, L.L., Hoover, C., Ostertag, S., Whalen, D., Pearced, T., Paulic, J., Iacozza, J., and MacPhee, S. 2018c. Beluga whales (Delphinapterus leucas), environmental change and marine protected areas in the Western Canadian Arctic. Estuar. Coast. Shelf Sci. 212: 128–137. doi: 10.1016/j.ecss.2018.05.026.
Lunn, N. J., Servanty, S., Regehr, E.V., Converse, S.J., Richardson, E. and Stirling, I. 2016. Demography of an apex predator at the edge of its range: Impacts of changing sea ice on polar bears in Hudson Bay. Ecol. Appl. 26: 1302–1320. doi: 10.1890/15-1256.
Marchese, C., Albouy, C., Tremblay, J.-É.., Dumont, D., D’Ortenzio, F., Vissault, S., and Bélanger, S. 2017. Changes in phytoplankton bloom phenology over the North Water (NOW) polynya: A response to changing environmental conditions. Polar Biol. 40: 1721–1737. doi: 10.1007/s00300-017-2095-2.
Matthews, C.J.D., Luque, S.P., Petersen, S.D., Andrews, R.D., and Ferguson, S.H. 2011. Satellite tracking of a killer whale (Orcinus orca) in the eastern Canadian Arctic documents ice avoidance and rapid, long-distance movement into the North Atlantic. Polar Biol. 34:1091–1096. doi: 10.1007/s00300-010-0958-x.
Matthews, C.J.D., Raverty, S.A., Noren, D.P., Arragutainaq, L., and Ferguson, S.H. 2019. Ice entrapment mortality may slow expanding presence of Arctic killer whales. Polar Biol. 42: 639–644. doi: 10.1007/s00300-018-02447-3.
McGhee, R. 1988. Beluga hunters: An archaeological reconstruction of the history and culture of the Mackenzie Delta Kittegaryumiut. Institute of Social and Economic Research, Memorial University of Newfoundland, St. John’s. 124 p.
McNicholl, D., and Dunmall, K. 2018a. Sachs Harbour coastal baseline July 2018. Available from https://www.facebook.com/arcticsalmon/photos/a.140681756049965/1850298851754905/?type=3&theater [accessed 08 February 2019].
McNicholl, D., and Dunmall, K. 2018b. Darnley Bay Coastal fish survey - July 3rd-18th, 2018. Available from https://tinyurl.com/Darnley-Bay-2018 [accessed 08 February 2019].
McNicholl, D.G., Johnson, J.D., and Reist, J.D. 2017. Darnley Bay nearshore survey: Synthesis of 2012 and 2014–2016 field programs. Can. Tech. Rep. Fish. Aquat. Sci. 3229: ix + 101 p. Available from http://publications.gc.ca/collections/collection_2017_mpo-dfo/Fs97-6-3229-eng.pdf [accessed 08 February 2019].
Merkel, F., Labansen, A.L., Boertmann, D., Mosbech, A., Egevang, C., Falk, K., Linnebjerg, J.F., Frederiksen, M., and Kampp, K. 2014. Declining trends in the majority of Greenland’s thick-billed murre (Uria lomvia) colonies 1981–2011. Polar Biol. 37: 1061–1071. doi: 10.1007/s00300-014-1500-3.
Michel, C., Hamilton, J., Hansen, E., Barber, D., Reigstad, M., Iacozza, J., Seuthe, L., and Niemi, A. 2015. Arctic Ocean outflow shelves in the changing Arctic: A review and perspectives. Prog. Oceanogr. 139: 66–88. doi: 10.1016/jpocean.2015.08.007.
Moore, S.E., and Huntington, H.P. 2008. Arctic marine mammals and climate change: Impacts and resilience. Ecol. Appl. 18: S157–S165. doi: 10.1890/06-0571.1.
Mueter, F., Nahrgang, J., Nelson, R.J., and Berge, J. 2016. The ecology of gadid fishes in the circumpolar Arctic with a special emphasis on the polar cod (Boreogadus saida). Polar Biol. 39: 961–967. doi: 10.1007/s00300-016-1965-3.
Mundy, C.J., Gosselin, M., Gratton, Y., Brown, K., Galindo, V., Campbell, K., Levasseur, M., Barber, D., Papkyriakou, T., and Bélanger, S. 2014. Role of environmental factors on phytoplankton bloom initiation under landfast sea ice in Resolute Passage, Canada. Mar. Ecol. Prog. Ser. 497: 39–49. doi: 10.3354/meps10587.
Nielsen, J.L., Ruggerone, G.T., and Zimmerman, C.E. 2013. Adaptive strategies and life history characteristics in a warming climate: Salmon in the Arctic? Environ. Biol. Fish. 96: 1187–1226. doi: 10.1007/s10641-012-0082-6.
Obbard, M.E., Cattet, M.R.L., Howe, E.J., Middel, K.R., Newton, E.J., Kolenosky, G.B., Abraham, K.F., and Greenwood, C.J. 2016. Trends in body condition in polar bears (Ursus maritimus) from the southern Hudson Bay subpopulation in relation to changes in sea ice. Arctic Science 2: 15–32. doi: 10.1139/as-2015-0027.
Obbard, M.E., Stapleton, S., Szor, G., Middel, K.R., Jutras, C., and Dyck, M. 2018. Re-assessing abundance of southern Hudson Bay polar bears by aerial survey: Effects of climate change at the southern edge of the range. Arctic Science 4: 634–655. doi: 10.1139/as-2018-0004.
Ostertag, S., Loseto, L., Snow, K., Lam, J., Hynes, K., and Gillman, V. 2018. “That’s how we know they’re healthy”: The inclusion of Indigenous Knowledge in beluga health monitoring in the Inuvialuit Settlement Region. Arctic Science 4: 292–320. doi: 10.1139/as-2017-0050.
Palmer, M.A., Saenz, B.T., and Arrigo, K.A. 2014. Impacts of sea ice retreat, thinning, and melt-pond proliferation on the summer phytoplankton bloom in the Chukchi Sea, Arctic Ocean. Deep Sea Res. II 105: 85–104. doi: 10.1016/j.dsr2.2014.03.016.
Pikialasorsuaq Commission. 2017. People of the ice bridge: The future of the Pikialasorsuaq. Report of the Pikialasorsuaq Commission. November 2017. 119 p. Available from http://www.pikialasorsuaq.org/en/Resources/Reports [accessed 09 February 2019].
Polar Knowledge Canada. 2017. Advancing polar science and collaboration: Polar Knowledge Canada report 2015–2017 (PDF, 3.19 MB). Polar Knowledge Canada, Ottawa, ON. 28 p.
Reist, J.D., Wrona, F.J., Prowse, T.D., Power, M., Dempson, J.B., King, J.R., and Beamish, R.J. 2006a. An overview of effects of climate change on selected Arctic freshwater and anadromous fishes. Ambio 35: 381–387. doi: 10.1579/0044-7447(2006)35%5B381:AOOEOC%5D2.0.CO;2.
Reist, J.D., Wrona, F.J., Prowse, T.D., Power, M., Dempson, J.B., Beamish, R.J., King, J.R., Carmichael, T.J., and Sawatzky, C.D. 2006b. General effects of climate change on Arctic fishes and fish populations. Ambio 35: 370–380. doi: 10.1579/0044-7447(2006)35[370:GEOCCO]2.0.CO;2.
Riedlinger, D., and Berkes, F. 2001. Contributions of traditional knowledge to understanding climate change in the Canadian Arctic. Polar Rec. 37: 315–328. doi: 10.1017/S0032247400017058.
RSEA. 2018. Beaufort Sea Regional Strategic Environmental Assessment.
https://rsea.inuvialuit.com.
Sciullo, L., Thiemann, G.W., and Lunn, N.J. 2016. Comparative assessment of metrics for monitoring the body condition of polar bears in western Hudson Bay. J. Zool. 300: 45–58. doi: 10.1111/jzo.12354.
Stevenson, M.G. 2004. Decolonizing co-management in northern Canada. Cultural Survival Quarterly 28-1: 68.
Stirling, I. 1997. The importance of polynyas, ice edges, and leads to marine mammals and birds. J. Mar. Syst. 10: 9–21. doi: 10.1016/S0924-7963(96)00054-1.
Stirling, I., Lunn, N. J., and Iacozza, J. 1999. Long-term trends in the population ecology of polar bears in Western Hudson Bay in relation to climatic change. Arctic 52: 294–306. doi: 10.14430/arctic935.
Syvitski, J.P.M., LeBlanc, K.W.G., and Cranston, R.E. 1990. The flux and preservation of organic carbon in Baffin Island fjords. Geol. Soc. London Spec. Publ. 53: 177–199. doi: 10.1144/GSL.SP.1990.053.01.10.
Towns, L., Derocher, A.E., Stirling, I., Lunn, N.J., and Hedman, D. 2009. Spatial and temporal patterns of problem bears in Churchill, Manitoba. Polar Biol. 32: 1529–1537. doi: 10.1007/s00300-009-0653-y.
Tremblay, J.-É., Michel, C., Hobson, K.A., Gosselin, M., and Price, N.M. 2006a. Bloom dynamics in early-opening waters of the Arctic Ocean. Limnol. Oceanogr. 51: 900–912. doi: 10.4319/lo.2006.51.2.0900.
Tremblay, J-É., Hattori, H., Michel, C., Ringuette, M., Mei, Z.-P., Lovejoy, C., Fortier, L., Hobson, K.A., Amiel, D., and Cochran, K. 2006b. Trophic structure and pathways of biogenic carbon flow in the eastern North Water Polynya. Prog. Oceanogr. 71: 402–425. doi: 10.1016/j.pocean.2006.10.006.
Tremblay, M., Frugal, C., Larrivee, C., Annanack, T., Tookalook, P., Qiisik, M., Angiyou, E., Swappie, N., Savard, J., and Barrett, M. 2008. Climate change in northern Quebec: Adaptation strategies from community-based research. Arctic 61: 27–34. doi: 10.14430/arctic99.
Watt, C.A., Orr, J., and Ferguson, S.H. 2016. A shift in foraging behaviour of beluga whales Delphinapterus leucas from the threatened Cumberland Sound population may reflect a changing Arctic food web. Endanger. Species Res. 31: 259–270. doi: 10.3354/esr00768.
Watt, C.A., Orr, J., and Ferguson, S.H. 2017. Spatial distribution of narwhal (Monodon monoceros) diving for Canadian populations helps identify important seasonal foraging areas. Can. J. Zool. 95: 41–50. doi: 10.1139/cjz-2016-0178.
Waugh, D., Pearce, T, Ostertag, S.K., Pokiak, V., Collings, P., and Loseto, L. 2018. Inuvialuit traditional ecological knowledge of beluga whale (Delphinapterus leucas) under changing climatic conditions in Tuktoyaktuk, NT. Arctic Science 4: 242–258. doi: 10.1139/as-2017-0034.
Westdal, K.H., Davies, J., MacPherson, A., Orr, J., and Ferguson, S.H. 2016a. Behavioural changes in belugas (Delphinapterus leucas) during a killer whale (Orcinus orca) attack in Southwest Hudson Bay. Can. Field-Nat. 130: 315–319. doi: 10.22621/cfn.v130i4.1925.
Westdal, K.H., Higdon, J.W., and Ferguson, S.H. 2016b. Review of killer whales (Orcinus orca) ice entrapments and ice-related mortality events in the northern hemisphere. Polar Biol. 40: 1467–1473. doi: 10.1007/s00300-016-2019-6.
White, G. 2006. Cultures in collision: Traditional knowledge and Euro-Canadian governance processes in native land-claim boards. Arctic 59: 401–414. doi: 10.14430/arctic289.
Worden, E. 2018. “Everything is changing so much”: Community Perspectives on the Declining Beluga Whale Harvest in Aklavik, NT. Thesis (M.Sc.) University of Manitoba, Winnipeg, MB. viii + 188 p. Available from https://mspace.lib.umanitoba.ca/xmlui/handle/1993/33654 [accessed 13 February 2019].
Yoon, S., Watanabe, E., Hiromichi, U., and Kishi, M.J. 2015. Potential habitat for chum salmon (Oncorhynchus keta) in the Western Arctic based on a bioenergetics model coupled with a three-dimensional lower trophic ecosystem model. Prog. Oceanogr. 131: 146–158. doi: 10.1016/j.pocean.2014.12.009.
Young, B.G., Higdon, J.W., and Ferguson, S.H. 2011. Killer whale (Orcinus orca) photo-identification in the eastern Canadian Arctic. Polar Res. 30: 7203. doi: 10.3402/polar.v30i0.7203.
Yurkowski, D.J., Auger‐Méthé, M., Mallory, M.L., Wong, S.N.P., Gilchrist, G., Derocher, A.E., Richardson, E., Lunn, N.J., Hussey, N.E., Marcoux, M., Togunov, R.R., Fisk, A.T., Harwood, L.A., Dietz, R., Rosing-Asvid, A., Born, E.W., Mosbech, A., Fort, J., Grémillet, D., Loseto, L., Richard, P.R., Iacozza, J., Jean-Gagnon, F., Brown, T.M., Westdal, K.H., Orr, J., LeBlanc, B., Hedges, K.J., Treble, M.A., Kessel, S.T., Blanchfield, P.J., Davis, S., Maftei, M., Spencer, N., McFarlane-Tranquilla, L., Montevecchi, W.A., Bartzen, B., Dickson, L., Anderson, C., and Ferguson, S.H. 2019. Abundance and species diversity hotspots of tracked marine predators across the North American Arctic. Divers. Distrib. 25: 328–345. doi: 10.1111/ddi.12860.
- Date de modification :